Bohri
| Bohri | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
107Bh
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Aspecte | |||||||||||||||||||||||||||||||||||||||||||
| Desconegut | |||||||||||||||||||||||||||||||||||||||||||
| Propietats generals | |||||||||||||||||||||||||||||||||||||||||||
| Nom, símbol, nombre | Bohri, Bh, 107 | ||||||||||||||||||||||||||||||||||||||||||
| Categoria d'elements | Metalls de transició | ||||||||||||||||||||||||||||||||||||||||||
| Grup, període, bloc | 7, 7, d | ||||||||||||||||||||||||||||||||||||||||||
| Pes atòmic estàndard | |||||||||||||||||||||||||||||||||||||||||||
| Configuració electrònica | [Rn] 5f14 6d5 7s2 (calculat) 2, 8, 18, 32, 32, 13, 2 (predit) 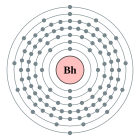
| ||||||||||||||||||||||||||||||||||||||||||
| Propietats físiques | |||||||||||||||||||||||||||||||||||||||||||
| Fase | Sòlid (predit) | ||||||||||||||||||||||||||||||||||||||||||
| Densitat (prop de la t. a.) |
37,1 (predit) g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||
| Propietats atòmiques | |||||||||||||||||||||||||||||||||||||||||||
| Estats d'oxidació | 7, 5, 4, 3 (predit) (només els estats d'oxidació en negreta es coneixen experimentalment) | ||||||||||||||||||||||||||||||||||||||||||
| Energies d'ionització (més) |
1a: 742,9 (estimat) kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||
| 2a: 1.688,5 (estimat) kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||
| 3a: 2.566,5 (estimat) kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||
| Radi atòmic | 128 (predit) pm | ||||||||||||||||||||||||||||||||||||||||||
| Radi covalent | 141 (estimat) pm | ||||||||||||||||||||||||||||||||||||||||||
| Miscel·lània | |||||||||||||||||||||||||||||||||||||||||||
| Estructura cristal·lina | Hexagonal compacta (predit) | ||||||||||||||||||||||||||||||||||||||||||
| Nombre CAS | 54037-14-8 | ||||||||||||||||||||||||||||||||||||||||||
| Isòtops més estables | |||||||||||||||||||||||||||||||||||||||||||
| Article principal: Isòtops del bohri | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
El bohri és un element químic sintètic el símbol del qual és Bh i el seu nombre atòmic és 107. Forma part del 7è període de la taula periòdica i és l'element més pesant del grup 7. Té aquest nom en honor de Niels Bohr. Els períodes de semidesintegració dels isòtops més estables són de l'ordre de només un minut.
Història
El bohri fou sintetitzat i identificat sense ambigüitat el 1981 per un equip de la Societat per a la Investigació en Ions Pesants (GSI) de Darmstadt, aleshores Alemanya Occidental, encapçalat per Gottfried Münzenberg. La reacció usada per a produir-lo havia estat proposada i aplicada el 1976 per un grup de l'Institut de Recerca Nuclear de Dubnà, aleshores Unió Soviètica, sota la direcció de Iuri Oganessian. Consistia a bombardejar blancs de bismut 209 i plom 208 amb nuclis accelerats de crom 54 i manganès 55, respectivament, per a produir bohri 262. Les reaccions proposades pels soviètics són:

L'equip alemany utilitzà bismut 209 i obtingué els isòtops bohri 260 i bohri 261, mitjançant el procés anomenat de fusió freda, que consisteix a fer que dos nuclis xoquin amb energies amb excitació baixa i, per tant, aprofitant la reducció de la tendència de desintegració d'aquests àtoms. Fou el primer element a sintetitzar-se d'aquesta manera. La reacció de síntesi del bohri 261 és:
A l'hora de buscar-li un nom, el grup alemany suggerí, el setembre de 1992, denominar-ho nielsbohri amb el símbol Ns per a honrar al físic danès Niels Bohr (1885-1962), un dels «pares» de la teoria quàntica. El 1994, un comitè de la Unió Internacional de Química Pura i Aplicada (IUPAC) recomanà anomenar-lo bohri i no nielsbohri. Els descobridors s'hi oposaren, perquè existia certa preocupació que el nom pogués confondre's amb el bor i, en particular, la distinció dels noms de les seves respectius oxoanions, bohrat i borat. L'assumpte es consultà a la secció danesa de la IUPAC que, malgrat aquest problema, votà a favor del nom bohri, i fou reconegut internacionalment el 1997.
Propietats
No s'han pogut determinar les propietats del bohri de forma experimental degut als baixos períodes de semidesintegració de tots els seus isòtops. Teòricament, s'han fet prediccions sobre les seves propietats i s'espera que sigui sòlid en condicions normals, que presenti una estructura cristal·lina hexagonal molt compacta (c/a = 1,62) i que el seu radi atòmic sigui al voltant dels 128 pm. A més, hauria de ser un metall molt pesant amb una densitat d'uns 37,1 g/cm³. Això es deu a l'elevada massa atòmica del bohri, a les contraccions de lantanoides i actinoides, i als efectes relativistes.
El bohri, amb configuració electrònica calculada , és el cinquè metall de transició del període 7 i el membre més pesant del grup 7 de la taula periòdica, sota el manganès, tecneci i reni. Tots ells presenten fàcilment l'estat d'oxidació +7, el qual es torna més estable a mesura que es descendeix en el grup. Per tant, s'espera que el bohri tengui un estat d'oxidació estable de +7, així com els estats inferiors +3 i +4. Els elements del seu grup formen heptaòxids volàtils, que en dissoldre's en aigua formen l'àcid corresponent. També es formen oxihalurs a partir de l'halogenació de l'òxid, per la qual cosa el bohri podria formar l'òxid volàtil , l'àcid perbòhric, i l'oxiclorur entre altres.
Isòtops
S'han descrit setze isòtops del bohri que han estat sintetitzats mitjançant la fusió freda de dos àtoms o mitjançant la descomposició d'elements més pesants. Tots els isòtops són radioactius, no té isòtops estables o naturals, i el seu isòtop conegut més estable, , té un període de semidesintegració d'aproximadament 61 s, encara que l'isòtop podria tenir, encara sense confirmar, un període de semidesintegració d'uns 690 s.
Els isòtops rics en protons amb nombres màssics 260, 261 i 262 es produïren directament per fusió freda; els que tenen nombres màssics 262 i 264 s'observaren en les cadenes de decadència del meitneri i del roentgeni. Per exemple el meitneri 266 dona el bohri 262 emetent una partícula alfa:
Els isòtops rics en neutrons amb nombres màssics 265, 266, 267 s'obtingueren en irradiacions de dianes d'actinoides. Els cinc més rics en neutrons amb nombres màssics 270, 271, 272, 274 i 278 (no confirmat) apareixen a les cadenes de decadència d'elements de nombre atòmic superior (nihoni, moscovi, tennes i flerovi), en concret , , , i respectivament. Així el dona per emissió de quatre partícules alfa segons la cadena:
Referències
- ↑ Johnson, E.; Fricke, B.; Jacob, T.; Dong, C. Z.; Fritzsche, S.; Pershina, V. «Ionization potentials and radii of neutral and ionized species of elements 107 (bohrium) and 108 (hassium) from extended multiconfiguration Dirac–Fock calculations». The Journal of Chemical Physics, 116, 2002, pàg. 1862. Bibcode: 2002JChPh.116.1862J. DOI: 10.1063/1.1430256.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Haire, Richard G. «Transactinides and the future elements». A: The Chemistry of the Actinide and Transactinide Elements. 3a edició. Dordrecht (Països Baixos): Springer Science+Business Media, 2006. ISBN 1-4020-3555-1.
- ↑ 3,0 3,1 Östlin, A.; Vitos, L. «First-principles calculation of the structural stability of 6d transition metals». Physical Review B, 84, 11, 2011. Bibcode: 2011PhRvB..84k3104O. DOI: 10.1103/PhysRevB.84.113104.
- ↑ Fricke, Burkhard «Superheavy elements: a prediction of their chemical and physical properties». Recent Impact of Physics on Inorganic Chemistry, 21, 1975, pàg. 89–144. DOI: 10.1007/BFb0116498 .
- ↑ Chemical Data. Bohrium - Bh, Royal Chemical Society
- ↑ Oganessian, Y. T.; Abdullin, F. S.; Bailey, P. D.; Benker, D. E.; Bennett, M. E.; Dmitriev, S. N.; Ezold, J. G.; Hamilton, J. H.; Henderson, R. A. «Synthesis of a New Element with Atomic Number Z=117». Physical Review Letters, 104, 14, 2010, pàg. 142502. Bibcode: 2010PhRvL.104n2502O. DOI: 10.1103/PhysRevLett.104.142502. PMID: 20481935. (dóna una semivida d'1,3 min basat en un sol esdeveniment; la conversió a semivida s'aconsegueix multiplicant per ln(2).)
- ↑ 7,0 7,1 FUSHE. «Synthesis of SH-nuclei», 2012.
- ↑ Münzenberg, G.; Hofmann, S.; Heßberger, F. P.; Reisdorf, W.; Schmidt, K. H. «Identification of element 107 byα correlation chains» (en anglès). Zeitschrift für Physik A Atoms and Nuclei, 300, 1, 01-03-1981, pàg. 107–108. DOI: 10.1007/BF01412623. ISSN: 0939-7922.
- ↑ Oganessian, Yu. Ts.; Demin, A. G.; Danilov, N. A.; Flerov, G. N.; Ivanov, M. P. «On spontaneous fission of neutron-deficient isotopes of elements 103, 105 and 107» (en anglès). Nuclear Physics A, 273, 2, 30-11-1976, pàg. 505–522. DOI: 10.1016/0375-9474(76)90607-2. ISSN: 0375-9474.
- ↑ 10,0 10,1 Moody, K.J.. «Synthesis of Superheavy Elements». A: Matthias Schädel, Dawn Shaughnessy. The Chemistry of Superheavy Elements (en anglès). 2a edició. Berlín: Springer Science & Business Media, 2014. ISBN 978-3-642-37466-1.
- ↑ «Bohrium - Element information, properties and uses | Periodic Table». .
- ↑ 12,0 12,1 12,2 12,3 Peña Zorrilla, A. «Z = 107, bohrio, Bh. Nombrado en honor del científico danés Niels Bohr». An. Quím., 115, 2, 2019, pàg. 169. Arxivat de l'original el 2020-02-07 .
- ↑ 13,0 13,1 Münzenberg, G.; Gupta, M. Production and Identification of Transactinide Elements (en anglès). Boston, MA: Springer US, 2011, p. 877–923. DOI 10.1007/978-1-4419-0720-2_19. ISBN 978-1-4419-0720-2.
- ↑ «Isotope data for meitnerium-266 in the Periodic Table». .
- ↑ «Isotope data for moscovium-287 in the Periodic Table». .
Enllaços externs
- webelements.com - Bohri (anglès)
- environmentalchemistry.com - Bohri (anglès)
| Taula periòdica | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||
















