메테인
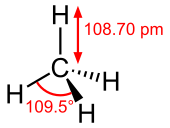
| |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN) | |||
| 체계명 | |||
별칭
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 3DMet | |||
| 1718732 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.739 | ||
| EC 번호 |
| ||
| 59 | |||
| KEGG | |||
| MeSH | Methane | ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1971 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| CH4 | |||
| 몰 질량 | 16.043 g·mol−1 | ||
| 겉보기 | 무색 기체 | ||
| 냄새 | Odorless | ||
| 밀도 | |||
| 녹는점 | −182.5 °C; −296.4 °F; 90.7 K | ||
| 끓는점 | −161.50 °C; −258.70 °F; 111.65 K | ||
| 임계점 (T, P) | 190.56 K, 4.5992 MPa | ||
| 22.7 mg·L−1 | |||
| 용해도 | 에탄올, 다이에틸 에터, 벤젠, 톨루엔, 메탄올, 아세톤에 대해 가용성, 물에 대해 불용성 | ||
| log P | 1.09 | ||
헨리 상수 (kH)
|
14 nmol·Pa−1·kg−1 | ||
| 짝산 | Methanium | ||
| 짝염기 | Methyl anion | ||
자화율 (χ)
|
−12.2×10−6 cm3·mol−1 | ||
| 구조 | |||
| Td | |||
| Tetrahedron | |||
| 0 D | |||
| 열화학 | |||
열용량 (C)
|
35.69 J·(K·mol)−1 | ||
표준 몰 엔트로피 (S
|
186.25 J·(K·mol)−1 | ||
표준 생성 엔탈피 (ΔfH⦵298)
|
−74.87 kJ·mol−1 | ||
표준 연소 엔탈피 (ΔcH⦵298)
|
−891.1 to −890.3 kJ·mol−1 | ||
| 위험 | |||
| GHS 그림문자 | 
| ||
| 신호어 | 위험 | ||
| H220 | |||
| P210 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | −188 °C (−306.4 °F; 85.1 K) | ||
| 537 °C (999 °F; 810 K) | |||
| 폭발 한계 | 4.4–17% | ||
| 관련 화합물 | |||
관련 알케인
|
|||
달리 명시된 경우를 제외하면, 표준상태(25 °C , 100 kPa)에서 물질의 정보가 제공됨.
| |||
메탄(독일어: Methan) 또는 메테인(영어: Methane 메세인[*] , CH
4)은 가장 간단한 탄소 화합물로, 탄소 하나에 수소 4개가 붙어 있다. 분자량은 16이다. 녹는점은 -183 °C, 끓는점은 -162 °C로 상온에서 기체이다.
자연적으로는 유기물이 물 속에서 부패, 발효할 때 생기므로 늪지대의 바닥 등에서 발생한다. 또 석탄층 속에 함유되어 석탄갱내에서 발생하여 공기와 섞여 폭발을 일으킬 때도 있다. 천연 가스나 석탄 가스의 주성분을 이룬다.
C-H의 결합 길이는 0.110nm이며, C-H의 결합 사이의 결합각은 109.5°이며, 무극성 분자이다.
순수한 메탄은 냄새가 없으나, 산업용으로 사용할 때 누출 여부 확인을 위해 냄새가 나는 다른 화합물을 일부 첨가하여 판매한다.
천연 가스의 주성분으로, 연료로 많이 사용된다. 메탄 분자 하나를 태우면 이산화 탄소 한 분자와 물 두 분자가 생성된다. 반응식은 다음과 같다.
- CH4 + 2O2 → CO2 + 2H2O
온실 효과의 원인이기도 하며, 같은 질량의 이산화 탄소보다 23배의 효과가 있다.
메테인의 치환반응
메테인은 햇빛존재하에 상온의 염소와 반응하여 치환 반응을 하는데, 중심의 탄소와 공유결합을 하고있는 수소가 차례로 염소와 치환되어 성질이 다른 분자로 바뀌어간다.
바뀌는 순서는 다음과 같다.
각주
- ↑ 가 나 〈Front Matter〉. 《Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 3–4쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
Methane is a retained name (see P-12.3) that is preferred to the systematic name ‘carbane’, a name never recommended to replace methane, but used to derive the names ‘carbene’ and ‘carbyne’ for the radicals H2C2• and HC3•, respectively.
- ↑ “Gas Encyclopedia”. 2018년 12월 26일에 원본 문서에서 보존된 문서. 2013년 11월 7일에 확인함.
- ↑ Pubchem. “Methane”. 《pubchem.ncbi.nlm.nih.gov》.
- ↑ “Safety Datasheet, Material Name: Methane” (PDF). USA: Metheson Tri-Gas Incorporated. December 4, 2009. June 4, 2012에 원본 문서 (PDF)에서 보존된 문서. December 4, 2011에 확인함.
- ↑ NOAA Office of Response and Restoration, US GOV. “METHANE”. 《noaa.gov》.
같이 보기
- 에테인
- 2023년 미국 텍사스 낙농장 폭발사고(en:2023 Texas dairy farm explosion) - 사고원인으로 메탄가스 추정


