Kaliumhyperoxid
In der heutigen Welt ist Kaliumhyperoxid ein interessantes Thema, das die Aufmerksamkeit vieler Menschen auf sich gezogen hat. Ob aufgrund seiner Relevanz in der Gesellschaft oder seiner Auswirkungen auf das tägliche Leben, Kaliumhyperoxid hat in verschiedenen Bereichen eine ständige Debatte ausgelöst. Von seinem Einfluss in der Politik bis zu seiner Präsenz im kulturellen Bereich ist es Kaliumhyperoxid gelungen, sich als Thema von unbestreitbarer Bedeutung zu positionieren. Im Laufe der Jahre hat sich Kaliumhyperoxid weiterentwickelt und an die sich ändernden Anforderungen der Gesellschaft angepasst, was es zu einem äußerst interessanten Thema macht, das einer eingehenden Analyse würdig ist. In diesem Artikel werden wir die verschiedenen Facetten von Kaliumhyperoxid und seine Auswirkungen auf die heutige Welt untersuchen.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
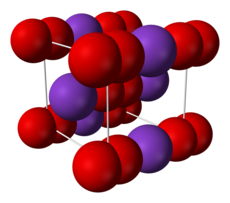
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kaliumhyperoxid | ||||||||||||||||||
| Andere Namen |
Kaliumsuperoxid | ||||||||||||||||||
| Summenformel | KO2 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 71,10 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,14 g·cm−3 | ||||||||||||||||||
| Schmelzpunkt |
380 °C | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Kaliumhyperoxid oder Kaliumsuperoxid (KO2) ist eine gelbe, salzartige chemische Verbindung und zählt zu den Hyperoxiden.
Eigenschaften und Verwendung
Das gelbe Salz zersetzt sich in Wasser lebhaft unter Bildung von Kalilauge, Wasserstoffperoxid und Sauerstoff.
- Kaliumhyperoxid reagiert mit Wasser unter Bildung von Kalilauge und Sauerstoff.
- Kaliumhyperoxid reagiert mit Wasser unter Bildung von Kalilauge und Wasserstoffperoxid.
Kaliumhyperoxid besitzt die Fähigkeit, Wasserdampf und Kohlenstoffdioxid zu binden und dafür Sauerstoff an die Umgebung abzugeben.
- Kaliumhyperoxid reagiert mit Kohlenstoffdioxid und Wasserdampf unter Bildung von Kaliumhydrogencarbonat und Sauerstoff.
Da sowohl Kohlenstoffdioxid als auch Wasser bei der Atmung abgegeben werden, kann es deshalb beispielsweise in Raumstationen, U-Booten oder in Atemrettungsgeräten zur Regenerierung der Atemluft verwendet werden.
Neben Kaliumhyperoxid wird zum Austausch von Kohlenstoffdioxid gegen Sauerstoff auch Natriumperoxid (Na2O2) benutzt.
Die Standardbildungsenthalpie von Kaliumhyperoxid beträgt ΔHf0 = -285 kJ/mol.
Darstellung
Kaliumhyperoxid wird durch Erhitzen von Kalium im Sauerstoffstrom oder in sauerstoffangereicherter Luft hergestellt. Es bildet sich allerdings auch nach folgender Reaktionsgleichung bei der Verbrennung von Kalium an der Luft unter Atmosphärendruck:
- Kalium reagiert mit Sauerstoff zu Kaliumhyperoxid.
Siehe auch
Einzelnachweise
- ↑ a b c d Datenblatt Kaliumhyperoxid bei Merck, abgerufen am 19. Januar 2011.
- ↑ a b Eintrag zu CAS-Nr. 12030-88-5 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 6. April 2011. (JavaScript erforderlich)
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1176.
Weblinks
- Oxide, Peroxide, Hyperoxide und Ozonide der Alkalimetalle: Herstellung, Struktur, Bedeutung ( vom 27. September 2007 im Internet Archive)





