Selenwasserstoff
In der heutigen Welt ist Selenwasserstoff ein Thema, das die Aufmerksamkeit von Millionen Menschen auf der ganzen Welt erregt hat. Seine Relevanz und Wirkung reichen von persönlichen bis hin zu globalen Aspekten und seine Auswirkungen sind in allen Bereichen des täglichen Lebens spürbar. Im Laufe der Zeit fordert Selenwasserstoff weiterhin die Grenzen des Wissens heraus und löst eine Debatte in der Gesellschaft aus. In diesem Zusammenhang ist es unerlässlich, dieses Thema umfassend zu erforschen, seine Auswirkungen zu verstehen und über seinen Einfluss auf unser Leben nachzudenken. In diesem Artikel tauchen wir in die faszinierende Welt von Selenwasserstoff ein, analysieren ihre vielen Facetten und entdecken, wie sie unsere Wahrnehmung und unser Handeln beeinflussen kann.
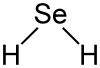
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Selenwasserstoff | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | H2Se | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 80,98 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt |
−66 °C | |||||||||||||||
| Siedepunkt | ||||||||||||||||
| Dampfdruck |
0,91 MPa bei 20 °C | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
| |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Selenwasserstoff, auch Monoselan, ist eine Verbindung aus Selen und Wasserstoff. Sie entsteht beim Auflösen salzartiger Selenide in verdünnten Säuren. Selenwasserstoff ist ein farbloses, äußerst giftiges Gas mit unangenehm fauligem Geruch. Bereits einmaliges Einatmen kleiner Mengen führt zu unangenehmen, lange anhaltenden Reizungen der Schleimhäute (sogenannter „Selenschnupfen“). Selenwasserstoff ist giftiger als Schwefelwasserstoff. Bei Laborversuchen, bei denen auch nur sehr geringe Mengen Selenwasserstoff entstehen, muss unbedingt unter einem Abzug gearbeitet werden und ein gasdichter Schutzanzug getragen werden.
Selenwasserstoff dient in der Halbleiter- und Elektronikindustrie zur Dotierung von Halbleitern.
Physikalische Eigenschaften

Selenwasserstoff ist gewinkelt gebaut (Bindungswinkel 91°), die Bindungslänge Se–H beträgt 146 pm.
| Eigenschaft | Wert |
|---|---|
| Kritische Temperatur | 138 °C |
| Kritischer Druck | 8,92 MPa |
| Kritische Dichte | 0,76 kg/l |
| Tripelpunkt Temperatur | −65,65 °C |
| Tripelpunkt Druck | 0,2738 bar |
Chemische Eigenschaften
Im Vergleich zu Schwefelwasserstoff ist Selenwasserstoff ein stärkeres Reduktionsmittel. Wässrige Lösungen von Selenwasserstoff reagieren mit Luftsauerstoff, wobei rotes Selen ausfällt.
Herstellung
Zu reinem Selenwasserstoff führt im Labor das Auflösen von trockenem Aluminiumselenid in Wasser, oder eine Reaktion der Elemente bei 400 °C:
Verwendung
Durch Reaktion mit einer Kaliumantimonyltartratlösung kann Antimon(III)-selenid hergestellt werden.
Weblinks
- Pocket Guide to Chemical Hazards für Hydrogen selenide bei dem National Institute for Occupational Safety and Health (NIOSH)
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Selenwasserstoff in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ P. G. Sennikov, V. E. Shkrunin, D. A. Raldugin, K. G. Tokhadze: Weak Hydrogen Bonding in Ethanol and Water Solutions of Liquid Volatile Inorganic Hydrides of Group IV-VI Elements (SiH4, GeH4, PH3, AsH3, H2S, and H2Se). 1. IR Spectroscopy of H Bonding in Ethanol Solutions in Hydrides. In: The Journal of Physical Chemistry. Band 100, Nr. 16, Januar 1996, S. 6415–6420, doi:10.1021/jp953245k.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 7783-07-5 bzw. Selenwasserstoff), abgerufen am 2. November 2015.
- ↑ Stoffliste (MAK-Werte und TRK-Werte), Verordnung des Bundesministers für Arbeit über Grenzwerte für Arbeitsstoffe sowie über krebserzeugende und fortpflanzungsgefährdende (reproduktionstoxische) Arbeitsstoffe (Grenzwerteverordnung 2021 – GKV), Österreich, abgerufen am 27. August 2021.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 627.
- ↑ a b Eintrag zu Selenwasserstoff. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Dezember 2014.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verbesserte und stark erweiterte Auflage. Walter de Gruyter, Berlin 1985, ISBN 3-11-007511-3, S. 528.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., Band 1, Academic Press 1963, S. 418–419.
- ↑ Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. Taylor & Francis US, 2011, ISBN 1-4398-1462-7, S. 39 (eingeschränkte Vorschau in der Google-Buchsuche).





