आयनिक यौगिक
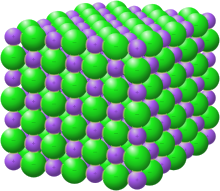
रासायनिकी में, आयनिक यौगिक या विद्युत्संयोजक यौगिक स्थिरवैद्युतिक बलों द्वारा एक साथ रखे गए आयनों से बना एक रासायनिक यौगिक होता है जिन्हें आयनी आबन्ध कहा जाता है। यौगिक समग्र रूप से तटस्थ है, किन्तु धनात्मक रूप से आवेशित आयनों को धनायन कहा जाता है और ऋणात्मक रूप से आवेशित आयनों को ऋणायन कहा जाता है। ये एकपारमाण्विक आयन हो सकते हैं जैसे सोडियम (Na + ) और Chloride (Cl-) सोडियम ख्लोराइड में, या बहुपरमाणुक प्रजातियाँ जैसे अमोनियम (NH+4) और कार्बोनेट (CO2−3) अमोनियम कार्बोनेट में आयन। ठोस होने पर आयनिक यौगिक साधारणतः क्रिस्टलीय संरचना बनाते हैं।
मूल आयन हाइड्रॉक्साइड (OH-) या ऑक्साइड (O2-) वाले आयनिक यौगिकों को क्षार के रूप में वर्गीकृत किया जाता है। इन आयनों के बिना आयनिक यौगिकों को लवण के रूप में भी जाना जाता है और अम्ल-क्षार अभिक्रियाओं द्वारा बनाया जा सकता है। आयनिक यौगिकों को उनके घटक आयनों से उनके विलायक , अवक्षेपण, हिमीकरण, एक ठोस-अवस्था अभिक्रिया, या अभिक्रियाशील अधातुओं जैसे कि हैलोजन गैसों के साथ अभिक्रियाशील धातुओं के इलेक्ट्रॉन स्थानान्तरण प्रतिक्रिया द्वारा भी उत्पादित किया जा सकता है।
आयनिक यौगिकों में साधारणतः उच्च गलनांक और क्वथनांक होते हैं, और कठोर और भंगुर होते हैं। ठोस के रूप में वे लगभग सदा विद्युद्रोधी होते हैं, लेकिन गलने या घुलने पर वे अत्यधिक प्रवाहकीय हो जाते हैं, क्योंकि आयन गतिशील होते हैं।
गुणधर्म
- भौतिक प्रकृति: धन एवं ऋण आयनों के मध्य शक्तिशाली आकर्षण बल के कारण आयनिक यौगिक ठोस एवं थोड़े कठोर होते हैं। ये यौगिक सामान्यतः भंगुर होते हैं तथा दाब डालने पर टुकड़ों में टूट जाते हैं।
- गलनांक एवं क्वथनांक: आयनिक यौगिकों का गलनांक एवं क्वथनांक अत्यधिक होता है, क्योंकि शक्तिशाली अन्तरायनिक आकर्षण को तोड़ने हेतु ऊर्जा की पर्याप्त मात्रा की आवश्यकता होती है।
- विलेयता: आयनिक यौगिक सामान्यतः जल में विलेय तथा केरोसीन, पेट्रोल आदि जैसे विलायकों में अविलेय होते हैं।
- विद्युत चालक्य: किसी विलयन से विद्युच्चालन के लिए आवेशित कणों की गतिशीलता आवश्यक होती है। आयनिक यौगिकों के जलीय विलयन में आयन उपस्थित होते हैं। जब विलयन में वैद्युतिक धारा प्रवाहित की जाती है तो यह आयन विपरीत इलेक्ट्रोड की ओर गमन करने लगते हैं। ठोसावस्था में आयनिक यौगिक विद्युच्चालन नहीं करते हैं, क्योंकि ठोसावस्था में दृढ़ संरचना के कारण आयनों की गति सम्भव नहीं होती है, किन्तु आयनिक यौगिक गलित अवस्था में विद्युच्चालन करते हैं, क्योंकि गलित अवस्था में विपरीत आवेश वाले आयनों के मध्य स्थिरवैद्युतिक आकर्षण बल ऊष्मा के कारण दुर्बल पड़ जाता है। इसलिए, आयन स्वतन्त्र रूप से गमन करते हैं एवं विद्युच्चालन करते हैं।
संरचना

आयनिक यौगिकों के क्रिस्टल में धनायन तथा ऋणायन त्रिविमीय रूप में नियमित रूप से व्यवस्थित रहते हैं। ये आयन कूलामी अन्योन्य बलों द्वारा परस्पर जुड़े रहते हैं। आयनों के आकार उनके नियचन क्रम तथा अन्य कारणों के आधार पर ये यौगिक विभिन्न क्रिस्टलीय संरचनाओं में क्रिस्टलित होते हैं।
आयनिक ठोस हेतु इलेक्ट्रॉन बन्धुता तथा आयनन ऊर्जा का योग धनात्मक हो सकता है। ऐसे में क्रिस्टल संरचना का स्थायित्व उसके जालक के बनने में उत्पन्न मुक्त ऊर्जा के कारण होता है। उदाहरणार्थ Na धातु से Na+ आयन के बनने की आयनन ऊर्जा 495.8 kJ/mol है, जबकि Cl से CI बनने की इलेक्ट्रॉन बन्धुता केवल - 348.7 kJ/mol है। इन दोनों का मान 147.1 kJ/mol होता है। यह परिमाण सोडियम ख्लोराइड के विरचन जालक ऊर्जा के मान (-788 J/mol) की अपेक्षा अधिक प्रतिपूरित होती है। इसी प्रकार सम्पूर्ण प्रक्रमों से प्राप्त होने वाली ऊर्जा शोषित ऊर्जा से कहीं अधिक होती है। अतः किसी आयनिक यौगिक के स्थायित्व का गुणात्मक मान उस यौगिक के विरचन जालक ऊर्जा के ऊपर निर्भर करती है, न कि गैस अवस्था में उस आयनिक प्रजाति द्वारा अष्टक प्राप्ति पर ।