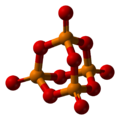
Dekatlenek tetrafosforu
W dzisiejszym świecie Dekatlenek tetrafosforu to temat, który zyskał duże znaczenie i przykuł uwagę szerokiego grona odbiorców. Wraz ze wzrostem znaczenia Dekatlenek tetrafosforu w naszym społeczeństwie istotne stało się zrozumienie jego implikacji i wpływu w różnych obszarach. Od poziomu osobistego po polityczny, Dekatlenek tetrafosforu wywołał intensywną debatę i promował ważne zmiany. W tym artykule dokładnie zbadamy znaczenie i implikacje Dekatlenek tetrafosforu, analizując jego ewolucję w czasie i jego wpływ na różne sfery współczesnego życia.
| |||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
P | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
P | ||||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa |
283,89 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
rozpływający się, biały lub prawie biały, bezpostaciowy proszek;bezwonny | ||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||
Dekatlenek tetrafosforu (potocznie: pięciotlenek fosforu; nazwa Stocka: tlenek fosforu(V)), P
4O
10 – nieorganiczny związek chemiczny z grupy tlenków kwasowych, w którym fosfor występuje na V stopniu utlenienia. Wzór empiryczny tego związku, P
2O
5, nie odzwierciedla jego prawdziwej struktury (typu adamantanu), z czterema atomami fosforu i dziesięcioma tlenu w cząsteczce (P
4O
10).
Otrzymuje się go, spalając fosfor w powietrzu. W temperaturze pokojowej ma postać śnieżnobiałego, drobnokrystalicznego proszku. Pod wpływem wilgoci łatwo ulega zbrylaniu. Prężność pary wodnej nad pięciotlenkiem fosforu wynosi mniej niż 1×10−5 Tr.
Reaguje gwałtownie z wodą, dając kwas ortofosforowy:
- P
4O
10 + 6H
2O → 4H
3PO
4
Ponadto jest zdolny do odwadniania kwasów mineralnych, tworząc ich bezwodniki:
Jest też zdolny do odwodnienia organicznego kwasu malonowego lub jego estrów, dając podtlenek węgla:
- CH
2(COOH)
2 + P
4O
10 → C
3O
2 + 4HPO
3
Zastosowanie
P
4O
10 stosowany jest:
- do otrzymywania kwasu ortofosforowego i jego soli, fosforanów,
- w technice laboratoryjnej jako środek suszący ze względu na swoją silną higroskopijność,
- jako herbicyd,
- jako nawóz do warzyw, kwiatów ogrodowych (w nawozach stężenie fosforu określa się jako procent P
2O
5, mimo że występuje on w postaci ortofosforanów), a jednocześnie środek do zwalczania szkodników,
- do usuwania smarów i innych substancji hydrofobowych,
- używany do produkcji Cl
2O
7 oraz fosforków metali przejściowych (np. Ni2P, Co2P, MoP), - razem z KI lub KBr do przekształcania alkoholi w odpowiednie jodki i bromki alkilu,
- razem z kwasem metanosulfonowym jako środek pomocniczy w reakcjach kondensacji.
Przypisy
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ a b c Phosphorus pentoxide, GESTIS-Stoffdatenbank, Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung, ZVG: 1850 (niem. • ang.).
- ↑ a b Dekatlenek tetrafosforu, Classification and Labelling Inventory, Europejska Agencja Chemikaliów (ang.).
- ↑ a b Pentatlenek fosforu (nr 431419) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. . (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Dekatlenek tetrafosforu (nr 431419) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. . (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ O. Diels, B. Wolf. Ueber das Kohlensuboxyd. I. „Berichte der deutschen chemischen Gesellschaft”. 39 (1), s. 689-697, 1906. DOI: 10.1002/cber.190603901103.
- ↑ A. Ellern, T. Drews, K. Seppelt. The Structure of Carbon Suboxide, C3O2, in the Solid State. „Zeitschrift für anorganische und allgemeine Chemie”. 627 (1), s. 73–76, 2001. DOI: 10.1002/1521-3749(200101)627:1<73::AID-ZAAC73>3.0.CO;2-A.
- ↑ podtlenek węgla, Encyklopedia techniki. Chemia, Władysław Gajewski (red.), Warszawa: Wydawnictwa Naukowo-Techniczne, 1965, s. 548, OCLC 33835352.
- ↑ a b c PubChem, Tetraphosphorus decaoxide , pubchem.ncbi.nlm.nih.gov (ang.).
- ↑ Produkcja roślinna Tom 1, wyd. II, Warszawa: Państwowe Wydawnictwo Rolnicze i Leśne, 1995
- ↑ a b c Phosphorus pentoxide , strona katalogowa produktu, MilliporeSigma (Merck KGaA) (ang.).