Elemento químico representativo
Neste artigo, exploraremos detalhadamente o tema Elemento químico representativo, um tema que tem despertado grande interesse e debate nos últimos tempos. Desde as suas origens até ao seu impacto na sociedade atual, Elemento químico representativo tem sido objeto de estudo e análise por especialistas de diversas disciplinas. Ao longo deste artigo examinaremos as diferentes perspectivas sobre Elemento químico representativo, bem como a sua relevância no contexto histórico e cultural. Além disso, nos aprofundaremos em aspectos específicos que ajudarão a compreender melhor a importância de Elemento químico representativo hoje, bem como suas possíveis implicações para o futuro. Prepare-se para mergulhar em uma viagem fascinante pelo universo de Elemento químico representativo!
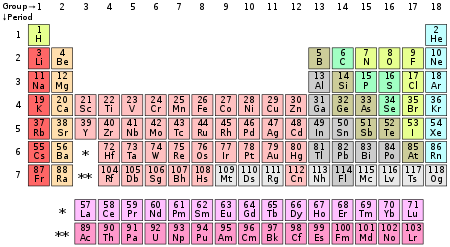
Elementos químicos representativos são, na química e física atômica, o grupo de elementos cujos membros mais leves são representados pelo hélio, lítio, berílio, boro, carbono, nitrogênio, oxigênio e flúor, como disposto na tabela periódica dos elementos. Os elementos representativos incluem os elementos (exceto o hidrogênio) dos grupos 1 e 2 (bloco s), e os grupos de 13 a 18 (bloco p). Os elementos do grupo 12 são considerados metais de transição; no entanto, zinco, cádmio, e mercúrio compartilham algumas propriedades com ambos os grupos (representativos e de transição), portanto alguns cientistas acreditam que eles devem ser incluídos no grupo dos elementos representativos.
Na Terra, os elementos representativos são os mais abundantes, bem como no Sistema Solar e no universo.
Configuração eletrônica
A configuração eletrônica dos elementos representativos apresenta o último nível com a seguinte distribuição:
- ns¹;
- ns², ou em
- ns² np1 a 5, onde n é o número quântico principal do último nível de energia.
Desta forma, temos:
- Metais alcalinos (grupo 1): ns¹
Ver também
Referências
- ↑ «Nomenclature of Inorganic Chemistry». International Union of Pure and Applied Chemistry. Consultado em 27 de setembro de 2011
- ↑ Jensen, William B. (2003). «The Place of Zinc, Cadmium, and Mercury in the Periodic Table» (PDF). Journal of Chemical Education. 80 (8): 952–561. Bibcode:2003JChEd..80..952J. doi:10.1021/ed080p952