Treonin
| Treonin | |
|---|---|
| C((C(=O)O)N)O | |
| Općenito | |
| Hemijski spoj | Treonin |
| Druga imena | 2-Amino-3-hidroksibutanoična kiselina |
| Molekularna formula | C4H9NO3 |
| CAS registarski broj | 80-68-2 |
| Osobine1 | |
| Molarna masa | 19.12 g mol−1 |
| Rastvorljivost | (H2O, g/dl) 10.6(30°),14.1(52°),19.0(61°) |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |


Treonin (Thr ili T) je esencijalna, polarna α - aminokiselina, sa formule HO2CCH(NH2)CH(OH)CH3. Zajedno sa serinom, treonin je jedan od proteinmogenih kiselina, a iako ima alkohol nu grupu, tirozin nije alkohol, već fenol, sa hidroksilnom grupom koja je direktno vezana za aromatični prsten, dajući mu različite kiseline / baze i oksidativna svojstva. To je također jedna od dvije zajedničke aminokiseline koje nose kiralni bočni lanac, zajedno sa izoleucinom. Njegovi kodoni su ACU, ACA, ACC, i ACG.
Treoninski ostatak je podložan brojnim posttranslacijskom modifikavijama e. U hidroksilnom bočnom lancu da povezano prođ O - O-glikolizaciju. Pored toga, treoninski ostaci prolaze kroz fosforilizaciju, uz djelovanje je treonin kinaze. U svom fosforiliziranom obliku, može se zvati fosfotreonin. Prekursor je glicina, a može se koristiti i kao prolek za pouzdano podizanje razine glicina u mozgu .
Historija
Treonin je otkrio William Cumming Rose (1930.), kao posljednju od standardnih 20 zajedničkih proteinogenih aminokiselina.
Stereoisomerizam
  |
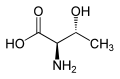
| L-Treonin (2S,3R) and D-Treonin (2R,3S) |
  |
| L-alo-Treonin (2S, 3S) i D-alo-Treonin (2R, 3R) |
Treonin je jedna od dvije proteinogena aminokiselina s dva hiralna centra. Može postojati u četiri moguća stereoizomera sa slijedećim konfiguracijama: (2s, 3R), (2R, 3s), ( 2s, 3s) i (2R , 3R ). Međutim, ime L-threonin se koristi za jedan jedini diastereomer – (2 s, 3R) - 2-amino-3-hydroxybutanoic kiselina. Drugi stereoizomer (2s, 3s), koji je rijetko prisutna u prirodi, se zove L- allo-treonin. Dva stereoizomera (2R, 3s) – i (2R, 3R)-2-amino-3-hidroksibutanoična kiselina su od manjeg značaja.
Biosinteza
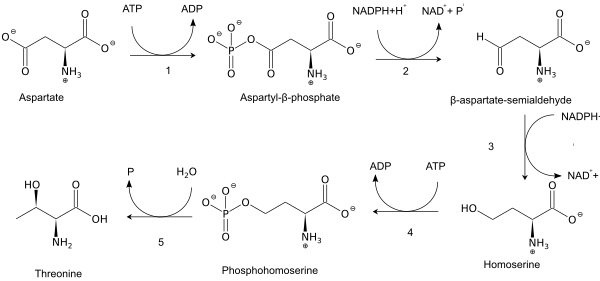
Kao esencijalna aminokiselina, treonin se ne sintetizira kod ljudi pa ga moramo unositi treonin u obliku proteina koji ga sadrže. U biljkama i mikroorganizmima, treonin se sintetizira od aspartamske kiseline, preko α-aspartil-semi- aldehid i homoserina. Homoserin prolazi kroz O-fosforilaciju; ovaj fosfatni ester prolazi hidrolizu istovremeno sa premještanjem OH grupe. U te procese biosinteze treonina uključučeni su:
- Aspartokinaza
- β-aspartat semi- aldehid dehidrogenaza
- Homoserin dehidrogenaza
- Homoserin kinaza
- Treonin sinteza.
Metabolizam
Treonin se metabolizira na dva načina:
- Pretvara se u piruvat, preko treonin dehidrogenaze. U ovom putu međuprodukti se mogu podvrgnuti tiolizi sa CoA, dajući acetil-CoA i glicin.
- Kod ljudi se pretvara u α-keto butirat – manji zajednički put preko enzima serin dehydrataza, čime ulazi u put koji vodi do sukcinil-CoA.
Izvori
Hrana bogata treonin uključuje kravlji sir, perad, riba, meso, sočivo, grah. i sjemenke susama. Racemski treonin se može pripremiti od krotonske kiseline u alfa funkciji, pomoću živinog (II) acetata.
Također pogledajte
Reference
- ^ Kornberg A. (1989): For the love of enzymes – The Odyssay of a biochemist. Harvard University Press, Cambridge (Mass.), London,ISBN 0-674-30775-5, ISBN 0-674-30776-3.
- ^ Graeme K. Hunter G. K. (2000): Vital Forces. The discovery of the molecular basis of life. Academic Press, London 2000, ISBN 0-12-361811-8.
- ^ Nelson D. L., Michael M. Cox M. M. (2013): Lehninger Biochemie. Springer, ISBN 978-3-540-68637-8.
- ^ Nelson D. L., Michael M. Cox M. M. (2013): Lehninger Principles of Biochemistry. W. H. Freeman, 2013.ISBN 978-1-4641-0962-1.
- ^ http://ndb.nal.usda.gov/ndb/foods/show/4632fg=&man=&lfacet=&count=&max=&sort=&qlookup=&offset=&format=Full&new=[mrtav link]
- ^ http://nutritiondata.self.com/.
Vanjski linkovi
- izvorima hrane od Treonin Arhivirano 30. 5. 2015. na Wayback Machine
- Treonin biosinteze
- CID 205
- CID 6288