Tumorski faktor nekroze
Tumorski faktor nekroze (TNF, kaheksin ili kahektin, zvani i tumorski faktor nekroze alfa ili TNF-α) citokinski mali protein koji koristi imunski sistem za ćelijsku signalizaciju. Ako makrofazi (određena bijela krvna zrnca) otkriju infekciju, oslobađaju TNF, kako bi upozorili druge ćelije imunskog sistema kao dio upalnog odgovora. TNF je član superporodica TNF, koja se sastoji od različitih transmembranskih proteina s homolognim domenom TNF.
TNF signalizacija javlja se putem dva receptora: TNFR1 i TNFR2. TNFR1 je konstitutivno eksprimiran na većini tipova ćelija, dok je TNFR2 ograničen prvenstveno na endotelne, epitelne i podskupine imunskih ćelija. Signalizacija TNF1 ima tendenciju da bude proupalna i apoptotska, dok je signalizacija TNFR2 protivupalna i podstiče ćelijsku proliferaciju. Suzbijanje signalizacije TNFR1 bilo je važno za liječenje autoimunske bolesti, dok signalizacija TNFR2 podstiče zacjeljivanje rana.
TNF-α postoji kao transmembranski oblik (mTNF-α) i kao topljivi oblik (sTNF-α). sTNF-α je rezultat enzimskog cijepanja mTNF-α. mTNF-α se uglavnom nalazi na monocitima/makrofazima, gdje stupa u interakciju s tkivnim receptorima, dodirom ćelija na ćeliju. sTNF-α se selektivno veže za TNFR1, dok se mTNF-α veže i za TNFR1 i za TNFR2. Vezivanje TNF-α za TNFR1 je ireverzibilno, dok je vezivanje za TNFR2 reverzibilno.
Primarna uloga TNF-a je u regulaciji imunskih ćelija. TNF, kao endogeni pirogen, može izazvati groznicu, apoptotsku ćelijsku smrt, kaheksiju, upalu i inhibirati tumorigenezu, replikaciju virusa, a i reagiraju na sepsu putem ćelijskih IL-1 i IL-6. Disregulacija proizvodnje TNF-a uključena je u različite ljudske bolesti, uključujući Alzheimerovu, kancer, glavnu depresiju, psorijazu i upalnu bolest crijeva (IBD). Iako kontroverzne, neke studije povezuju depresiju i IBD s povećanim nivoom TNF -a.
Pod imenom tasonermin, TNF se koristi kao imunostimulacijski lijek u liječenju određenih karcinoma. Lijekovi koji se suprotstavljaju djelovanju TNF-a koriste se u liječenju različitih upalnih bolesti, naprimjer reumatoidnog artritisa.
Određeni karcinomi mogu uzrokovati hiperprodukciju TNF-a. TNFsu paralele paratireoidnih hormona i u izazivanju sekundarne hiperkalcemije i u raku s kojim je povezana prekomerna proizvodnja.
Otkriće
Teoriju antitumorskog odgovora imunskog sistema in vivo otkrio je ljekar William B. Coley. u 1968, Gale A Granger sa Univerziteta Kalifornija, Irvine, prijavio citotoksični faktor kojeg proizvode limfociti i nazvao ga limfotoksin (LT). Zaslugu za ovo otkriće dijeli Nancy H. Ruddle sa Univerziteta Yale, koja je prijavila istu aktivnost u sekvenci leđa-leđa objavljenih u istom mjesecu. Nakon toga, 1975. Lloyd J. Old iz Memorial Sloan-Kettering Cancer Center, New York, izvijestio je o drugom citotoksičnom faktoru kojegh proizvode makrofazi i nazvao ga faktor tumorske nekroze (TNF). Oba faktora su opisana na osnovu njihove sposobnosti da ubiju mišje fibrosarkomske ćelije L-929. Ovi koncepti su prošireni na sistemske bolesti 1981. godine, kada je Ian A. Clark, sa Australian National University, u saradnji sa Elizabeth Carswell iz Oldove grupe, radio na podacima iz doba sekvenciranja, obrazložio da prekomjerna proizvodnja TNF-a uzrokuje bolest malarija i trovanje endotoksinom.
cDNK kodirajući LT i TNF su klonirani u 1984 i otkriveno je da su slični. Vezivanje TNF -a za njegov receptor i njegovo pomicanje pomoću LT potvrdilo je funkcionalnu homologiju između dva faktora. Sekvencna i funkcionalna homologija TNF-a i LT-a dovela je do preimenovanja TNF-a u TNFα i LT u TNFβ. U 1985. Bruce A. Beutler i Anthony Cerami otkrili su da je kahektin (hormon koji inducira kaheksiju) zapravo TNF. Zatim su identificirali TNF kao posrednika u trovanju smrtonosnim endotoksinom. Kevin J. Tracey i Cerami otkrili su ključnu posredničku ulogu TNF-a u smrtonosnom sepsnom šoku i identificirali terapeutske učinke monoklonskih anti-TNF antitijela.
Istraživanja u Laboratoriji Marka Mattsona pokazala su da TNF može spriječiti smrt/apoptozu neurona mehanizmom koji uključuje aktivaciju transkripcijskog faktora NF-κB, koji inducira ekspresiju antioksidativnih enzima i Bcl-2.
Aminokiselinska sekvenca
Dužina polipeptidnog lanca je 233 aminokiseline, a molekulska težina 25.644 Da..
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MSTESMIRDV | ELAEEALPKK | TGGPQGSRRC | LFLSLFSFLI | VAGATTLFCL | ||||
| LHFGVIGPQR | EEFPRDLSLI | SPLAQAVRSS | SRTPSDKPVA | HVVANPQAEG | ||||
| QLQWLNRRAN | ALLANGVELR | DNQLVVPSEG | LYLIYSQVLF | KGQGCPSTHV | ||||
| LLTHTISRIA | VSYQTKVNLL | SAIKSPCQRE | TPEGAEAKPW | YEPIYLGGVF | ||||
| QLEKGDRLSA | EINRPDYLDF | AESGQVYFGI | IAL |
Gen
Ljudski TNF gen je kloniran 1985. godine. Mapiran je na hromosomu 6, p21.3, obuhvatajući približno 3 kB i sadrži 4 egzona. Posljednji egzon ima sličnost sa limfotoksinom alfa (LTA, ranije imenovan kao TNF-β). Tri glavna netranslatirana područja (3'-UTR) TNF-a sadrži AU-bogati element (ARE).
Struktura
TNF se prvenstveno proizvodi kao 233 aminokiseline dugi transmembranski protein tipa II raspoređen u stabilne homotrimere. Iz ovog membranski integriranog oblika, oslobađa se rastvorljivi homotrimerni citokin (sTNF), proteolitskim cijepanjem pomoću enzima koji pretvara TNF alfa-metaloproteazu (TACE, također zvana ADAM17). Rastvorljivi trimerni sTNF od 51 kDa ima tendenciju disocijacije pri koncentracijama ispod nanomolarnog raspona, čime se gubi njegova bioaktivnost. Izlučeni oblik ljudskog TNF-a poprima oblik trokutaste piramide i teži oko 17 kDa. I izlučeni i membranski vezani oblici su biološki aktivni, iako su specifične funkcije svakog od njih kontroverzne. No, oba oblika imaju preklapajuće i različite biološke aktivnosti.
TNF običnog kućnog miša i ljudski TNF strukturno se razlikuju. TNF protomori, dugi 17 kDa (185 aminokiselina) sastavljeni su od dva antiparalelna β-nabrana lista sa antiparalelnim β-lacima, tvoreći β-strukturu 'žele valjaka', tipsku za porodicu TNF, ali se također nalazi u proteinima virusne kapside.
Ćelijska signalizacija
TNF može vezati dva receptora, TNFR1 (TNF receptor tip 1; CD120a; p55/60) i TNFR2 (TNF receptor tip 2; CD120b; p75/80). TNFR1 je 55 kDa, a TNFR2 75 kDa. TNFR1 je eksprimiran u većini tkiva i može se u potpunosti aktivirati i membranski vezanim i rastvorljivim trimernim oblicima TNF-a, dok se TNFR2 obično nalazi u ćelijama imunskog sistema i reagira na membranski vezan oblik TNF homotrimer. Kako je većina informacija o TNF-signalizaciji izvedena iz TNFR1, uloga TNFR2 je vjerojatno potcijenjena. Barem djelomično jer TNFR2 nema unutarćelijski domen smrti, pokazuje neuroprotektivna svojstva.
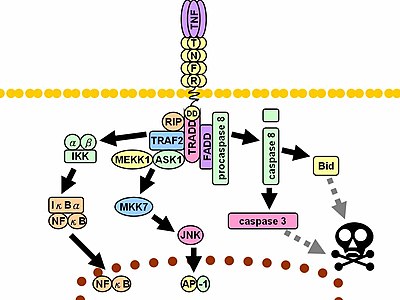
Nakon kontakta sa svojim ligandom, TNF receptori također formiraju trimere, čiji se vrhovi uklapaju u utore formirane između TNF monomera. Ovo vezivanje uzrokuje konformacijsku promjenu u receptoru, što dovodi do disocijacije inhibitornog proteina SODD iz domena unutaćelijske smrti. Ova disocijacija omogućava adapterskom proteinu TRADD da se veže za domen smrti, služeći kao platforma za kasnije vezivanje proteina. Nakon vezanja TRADD-a, mogu se pokrenuti tri puta.
- Aktiviranje NF-κB: TRADD regrutira TRAF2 i RIP. TRAF2 zauzvrat regrutira višekomponentni protein kinaza IKK, omogućavajući serin-treonin kinazama RIP da ga aktivira. Inhibitorni protein, IκBα, koji se normalno veže za NF-κB i inhibira njegovu translokaciju, fosforiliranjem pomoću IKK-a, a zatim se razgrađuje, oslobađajući NF-κB. NF-κB je heterodimerni transkripcijski faktor koji se translocira u jedro i posreduje u transkripciji velikog broja proteina uključenih u preživljavanje i proliferaciju ćelija, upalni odgovor i apoptotski faktori.
- Aktivacija MAPK puteva: Od tri velike kaskade MAPK, TNF izaziva snažnu aktivaciju stres-vezanih JNK grupa, izazivajući umjeren odgovor p38-MAPK i odgovorna je za minimalnu aktivaciju klasičnih ERK. TRAF2/Rac aktivira JNK-inducirajuće kinaze inducirane putemMLK2/MLK3, TAK1, MEKK1 i ASK1 (bilo direktno ili putem GCK-a i Trx-a). Osa SRC-Vav-Rac aktivira MLK2/MLK3 i ove kinaze fosforila MKK7, koja zatim aktivira JNK. JNK prelazi u jedro i aktivira transkripcijske faktore kao što su c-jun i ATF2. Put JNK je uključen u ćelijsku diferencijaciju, proliferaciju i općenito je pro-apoptozan.
- Indukcija signalizacije ćelijske smrti: Kao i svi članovi superporodice TNFR koji sadrže domen smrti, TNFR1 je uključen u signalizaciju smrti. Međutim, ćelijska smrt inducirana TNF-om ima samo manju ulogu u usporedbi s njenom snažnom funkcijom u upalnom procesu. Njegova sposobnost izazivanja smrti je slaba u poređenju s drugim članovima porodice (kao što je Fas) i često je prikrivena anti-apoptotskim efektima NF-κB. Ipak, TRADD veže FADD, koji zatim regrutuje cistein-proteazu kaspazu-8. Visoka koncentracija kaspaze-8 inducira njenu autoproteolitsku aktivaciju i naknadno cijepanje efektora kaspaza, što dovodi do ćelijske apoptoze.
Nebrojeni i često sukobljeni efekti posredovani gore navedenim putevima ukazuju na postojanje opsežnog unakrsnog uticaja. Naprimjer, NF-κB pojačava transkripciju C-FLIP, Bcl-2 i cIAP1 / cIAP2, inhibitornih proteina koji ometaju signalizaciju smrti . S druge strane, aktivirane kaspaze cijepaju nekoliko komponenti puta NF-κB, uključujući RIP, IKK i podjedinice samog NF-κB. Drugi faktori, poput tipa ćelije, istovremene stimulacije drugih citokina ili količine reaktivnih vrsta kisika (ROS) mogu promijeniti ravnotežu u korist jednog ili drugog puta. Takva komplicirana signalizacija osigurava da, kad god se TNF oslobodi, različite ćelije s izrazito različitim funkcijama i stanjima mogu na odgovarajući način reagirati na upalu. Faktori tumorske nekroze alfa i keratin 17mogu biti povezani u slučaju oralne submukozne fibroze,
Postoje i dokazi da signalizacija TNF-α izaziva nizvodne epigenetičke modifikacije koje rezultiraju trajnim poboljšanjem proupalnih odgovora u ćelijama.
Enzimska regulacija
Ovaj protein može koristiti morfeinski model alosterne regulacije.
Fiziologija
Smatralo se da TNF prvenstveno proizvode makrofazi, ali ga proizvodi i veliki broj tipova ćelija, uključujući limfoidne, mastocite, endotelne, srčani miociti, masno tkivo , fibroblasti i neuroni. Velike količine TNF-a oslobađaju se kao odgovor na lipopolisaharidne, druge bakterijske 1 proizvode i interleukin-1 (IL-1). U koži su mastociti dominantni izvor prethodno formiranog TNF-a, koji se može osloboditi nakon upalnog podražaja (npr. LPS).
Ima niz djelovanja na različite organske sisteme, općenito zajedno s IL-1 i interleukin-6 (IL-6):
- Na hipotalamusu:
- Stimulacija hipotalamusno-hipofizno-nadbubrežne osi, stimulacijom otpuštanja kortikotropin oslobađajućeg hormona (CRH)
- Suzbijanje apetita
- Vrućica
- Na jetri: stimulacija akutne faze odgovora, što dovodi do povećanja C-reaktivnog proteina i niza drugih medijatora. Također inducira inzulinsku rezistenciju podsticanjem fosforilacije serinskog supstrata insulinskog receptora-1 (IRS-1), što narušava signalizaciju insulina
- To je moćan hemoatraktant za neutrofileds i potiče ekspresiju adhezijskih molekula na endotelnim ćelijama, pomažući u migraciji neutrofila.
- Na makrofagima: stimulira fagocitozu i proizvodnju oksidanata IL-1 i upalnih lipida prostaglandin E2 (PGE2)
- Na drugim tkivima: povećanje insulinska rezistencije. TNF fosforilira ostatke serinskih receptora insulina, blokirajući transdukciju signala.
- U metabolizmu i unosu hrane: regulira percepciju gorkog okusa.
Lokalno povećanje koncentracije TNF -a uzrokovat će kardinalne znakove upale: vrućinu, oteklinu, crvenilo, bol i gubitak funkcije.
Dok visoke koncentracije TNF-a izazivaju simptome slične šoku, produžena izloženost niskim koncentracijama TNF-a može rezultirati kaheksijom, sindromom trošenja. Ovo se može naći, naprimjer, kod pacijenata sa kancerom.
Said et al. pokazali su da TNF uzrokuje IL-10-ovisnu inhibiciju ekspanzije i funkcije CD4 T-ćelija, reguliranjem povećane razine PD-1 na monocitima, što dovodi do proizvodnje IL-10 u monocitima, nakon vezivanja PD-1 za PD-L.
Istraživanje Pedersena et al. ukazuje da je povećanje TNF-a kao odgovora na sepsu inhibiranog proizvodnjom miokina induciranih vježbom. Da bi se ispitalo izaziva li akutna vježba pravi protivupalni odgovor, uspostavljen je model „upale niskog stupnja“ u kojem je niska doza endotoksina E. coli primijenjena na zdrave dobrovoljce, koji su randomizirani na odmor ili vježbanje prije primjene endotoksina. Kod ispitanika u mirovanju, endotoksin je inducirao dva do tri puta povećanje cirkulirajućeg nivoa TNF-a. Nasuprot tome, kada su ispitanici izveli tri sata vožnje na ergometru i primili endotoksinski bolus nakon 2,5 sata, odgovor na TNF bio je potpuno prigušen. Ova studija pruža neke dokaze da akutna vježba može spriječiti proizvodnju TNF -a.
Farmakologija
TNF podstiče upalni odgovor, koji zauzvrat uzrokuje mnoge kliničke probleme povezane s autoimunskim poremećajima, kao što su reumatoidni artritis, ankilozantni spondilitis, upalna bolest crijeva, psorijaza , hidradenitis suppurativa i vatrostalna astma. Ovi se poremećaji ponekad liječe upotrebom TNF inhibitora. Ova inhibicija se može postići monoklonskim antitijelima, kao što je infliksimab (Remicade), koji se direktno vežu za TNF, adalimumab (Humira), certolizumab pegol (Cimzia) ili s mamcem cirkulacijski receptor fuzijski protein kao što je etanercept (Enbrel) koji se veže za TNF s većim afinitetom od TNFR -a.
S druge strane, neki pacijenti liječeni inhibitorima TNF-a imaju pogoršanje svoje bolesti ili novi početak autoimunosti. Čini se da TNF ima i imunosupresivni aspekt. Jedno objašnjenje mogućeg mehanizma je ovo zapažanje da TNF ima pozitivan učinak na regulatorne T-ćelije (Tregs), zbog svog vezivanja za receptor 2 faktora nekroze tumora (TNFR2).
Anti-TNF terapija pokazala je samo skromne efekte u terapiji raka. Liječenje karcinoma bubrežnih ćerlija infliksimabom rezultiralo je produženom stabilizacijom bolesti kod određenih pacijenata. Etanercept je testiran za liječenje pacijenata s rakom dojke i rakom jajnika, koji pokazuju produženu stabilizaciju bolesti kod određenih pacijenata, putem snižavanja IL-6 i CCL2 . S druge strane, dodavanje infliximaba ili etanercepta u gemcitabin za liječenje pacijenata s uznapredovalim rakom gušterače nije povezano s razlikama u učinkovitosti u usporedbi s placebom.
Interakcije
Pokazano je da TNF komunicira sa TNFRSF1A.
Nomenklatura
Zato što se LTα više ne naziva TNFβ, TNFα, kao prethodni simbol gena, sada se jednostavno naziva TNF, kako je prikazano u bazi podataka HGNC (HUGO odbor za nomenklaturu gena).
Reference
- ^ a b c ENSG00000230108, ENSG00000223952, ENSG00000204490, ENSG00000228321, ENSG00000232810, ENSG00000228849, ENSG00000206439 GRCh38: Ensembl release 89: ENSG00000228978, ENSG00000230108, ENSG00000223952, ENSG00000204490, ENSG00000228321, ENSG00000232810, ENSG00000228849, ENSG00000206439 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000024401 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c Heir R, Stellwagen D (2020). "TNF-Mediated Homeostatic Synaptic Plasticity: From in vitro to in vivo Models". Frontiers in Cellular Neuroscience. 14: 565841. doi:10.3389/fncel.2020.565841. PMC 7556297. PMID 33192311.
- ^ a b c d Gough P, Myles IA (2020). "Tumor Necrosis Factor Receptors: Pleiotropic Signaling Complexes and Their Differential Effects". Frontiers in Immunology. 11: 585880. doi:10.3389/fimmu.2020.585880. PMC 7723893. PMID 33324405.
- ^ Rolski F, Błyszczuk P (2020). "Complexity of TNF-α Signaling in Heart Disease". Journal of Clinical Medicine. 9 (10): 3267. doi:10.3390/jcm9103267. PMC 7601316. PMID 33053859.
- ^ a b Probert L (2017). "Forward and Reverse Signaling Mediated by Transmembrane Tumor Necrosis Factor-Alpha and TNF Receptor 2: Potential Roles in an Immunosuppressive Tumor Microenvironment". Frontiers in Immunology. 8: 1675. doi:10.3389/fimmu.2017.01675. PMC 5712345. PMID 29234328.
- ^ Rolski F, Błyszczuk P (2015). "TNF and its receptors in the CNS: The essential, the desirable and the deleterious effects". Neuroscience. 302: 2–22. doi:10.1016/j.neuroscience.2015.06.038. PMID 26117714.
- ^ Szondy Z, Pallai A (2017). "Transmembrane TNF-alpha reverse signaling leading to TGF-beta production is selectively activated by TNF targeting molecules: Therapeutic implications". Pharmacological Research. 115: 124–132. doi:10.1016/j.phrs.2016.11.025. PMID 27888159.
- ^ Swardfager W, Lanctôt K, Rothenburg L, Wong A, Cappell J, Herrmann N (2010). "A meta-analysis of cytokines in Alzheimer's disease". Biol Psychiatry. 68 (10): 930–941. doi:10.1016/j.biopsych.2010.06.012. PMID 20692646. S2CID 6544784.
- ^ Locksley RM, Killeen N, Lenardo MJ (2001). "The TNF and TNF receptor superfamilies: integrating mammalian biology". Cell. 104 (4): 487–501. doi:10.1016/S0092-8674(01)00237-9. PMID 11239407. S2CID 7657797.
- ^ Dowlati Y, Herrmann N, Swardfager W, Liu H, Sham L, Reim EK, Lanctôt KL (2010). "A meta-analysis of cytokines in major depression". Biol Psychiatry. 67 (5): 446–457. doi:10.1016/j.biopsych.2009.09.033. PMID 20015486. S2CID 230209.
- ^ Victor FC, Gottlieb AB (2002). "TNF-alpha and apoptosis: implications for the pathogenesis and treatment of psoriasis". J Drugs Dermatol. 1 (3): 264–75. PMID 12851985.
- ^ Brynskov J, Foegh P, Pedersen G, Ellervik C, Kirkegaard T, Bingham A, Saermark T (2002). "Tumour necrosis factor alpha converting enzyme (TACE) activity in the colonic mucosa of patients with inflammatory bowel disease". Gut. 51 (1): 37–43. doi:10.1136/gut.51.1.37. PMC 1773288. PMID 12077089.
- ^ Mikocka-Walus AA, Turnbull DA, Moulding NT, Wilson IG, Andrews JM, Holtmann GJ (2007). "Controversies surrounding the comorbidity of depression and anxiety in inflammatory bowel disease patients: a literature review". Inflammatory Bowel Diseases. 13 (2): 225–234. doi:10.1002/ibd.20062. PMID 17206706.
- ^ Bobińska K, Gałecka E, Szemraj J, Gałecki P, Talarowska M (2017). "Is there a link between TNF gene expression and cognitive deficits in depression?". Acta Biochim. Pol. 64 (1): 65–73. doi:10.18388/abp.2016_1276. PMID 27991935.
- ^ Kolb WP, Granger GA (1968). "Lymphocyte in vitro cytotoxicity: characterization of human lymphotoxin". Proc. Natl. Acad. Sci. U.S.A. 61 (4): 1250–5. Bibcode:1968PNAS...61.1250K. doi:10.1073/pnas.61.4.1250. PMC 225248. PMID 5249808.
- ^ Ruddle NH, Waksman BH (decembar 1968). "Cytotoxicity mediated by soluble antigen and lymphocytes in delayed hypersensitivity. 3. Analysis of mechanism". J. Exp. Med. 128 (6): 1267–79. doi:10.1084/jem.128.6.1267. PMC 2138574. PMID 5693925.
- ^ Carswell EA, Old LJ, Kassel RL, Green S, Fiore N, Williamson B (1975). "An endotoxin-induced serum factor that causes necrosis of tumors". Proc. Natl. Acad. Sci. U.S.A. 72 (9): 3666–70. Bibcode:1975PNAS...72.3666C. doi:10.1073/pnas.72.9.3666. PMC 433057. PMID 1103152.
- ^ Clark IA, Virelizier JL, Carswell EA, Wood PR (juni 1981). "Possible importance of macrophage-derived mediators in acute malaria". Infect. Immun. 32 (3): 1058–66. doi:10.1128/IAI.32.3.1058-1066.1981. PMC 351558. PMID 6166564.
- ^ Clark IA (juli 1982). "Suggested importance of monokines in pathophysiology of endotoxin shock and malaria". Klin. Wochenschr. 60 (14): 756–8. doi:10.1007/BF01716573. PMID 6181289. S2CID 26446784.
- ^ Pennica D, Nedwin GE, Hayflick JS, Seeburg PH, Derynck R, Palladino MA, Kohr WJ, Aggarwal BB, Goeddel DV (1984). "Human tumour necrosis factor: precursor structure, expression and homology to lymphotoxin". Nature. 312 (5996): 724–9. Bibcode:1984Natur.312..724P. doi:10.1038/312724a0. PMID 6392892. S2CID 4245957.
- ^ Beutler B, Greenwald D, Hulmes JD, Chang M, Pan YC, Mathison J, Ulevitch R, Cerami A (1985). "Identity of tumour necrosis factor and the macrophage-secreted factor cachectin". Nature. 316 (6028): 552–4. Bibcode:1985Natur.316..552B. doi:10.1038/316552a0. PMID 2993897. S2CID 4339006.
- ^ Beutler B, Milsark IW, Cerami AC (august 1985). "Passive immunization against cachectin/tumor necrosis factor protects mice from lethal effect of endotoxin". Science. 229 (4716): 869–71. Bibcode:1985Sci...229..869B. doi:10.1126/science.3895437. PMID 3895437.
- ^ Tracey KJ, Beutler B, Lowry SF, Merryweather J, Wolpe S, Milsark IW, Hariri RJ, Fahey TJ, Zentella A, Albert JD (oktobar 1986). "Shock and tissue injury induced by recombinant human cachectin". Science. 234 (4775): 470–74. Bibcode:1986Sci...234..470T. doi:10.1126/science.3764421. PMID 3764421.
- ^ Tracey KJ, Fong Y, Hesse DG, Manogue KR, Lee AT, Kuo GC, Lowry SF, Cerami A (decembar 1987). "Anti-cachectin/TNF monoclonal antibodies prevent septic shock during lethal bacteraemia". Nature. 330 (6149): 662–64. Bibcode:1987Natur.330..662T. doi:10.1038/330662a0. PMID 3317066. S2CID 4308324.
- ^ Mattson MP, Meffert MK (2006). "Roles for NF-kappaB in nerve cell survival, plasticity, and disease". Cell Death & Differentiation. 13 (5): 852–860. doi:10.1038/sj.cdd.4401837. PMID 16397579.
- ^ a b Chadwick W, Magnus T, Mattson MP, Maudsley S (2008). "Targeting TNF-alpha receptors for neurotherapeutics". Trends in Neurosciences. 31 (10): 504–511. doi:10.1016/j.tins.2008.07.005. PMC 2574933. PMID 18774186.
- ^ "UniProt, P01375". Pristupljeno 19. 8. 2021.
- ^ Old LJ (1985). "Tumor necrosis factor (TNF)". Science. 230 (4726): 630–2. Bibcode:1985Sci...230..630O. doi:10.1126/science.2413547. PMID 2413547.
- ^ Nedwin GE, Naylor SL, Sakaguchi AY, Smith D, Jarrett-Nedwin J, Pennica D, Goeddel DV, Gray PW (1985). "Human lymphotoxin and tumor necrosis factor genes: structure, homology and chromosomal localization". Nucleic Acids Res. 13 (17): 6361–73. doi:10.1093/nar/13.17.6361. PMC 321958. PMID 2995927.
- ^ Kriegler M, Perez C, DeFay K, Albert I, Lu SD (1988). "A novel form of TNF/cachectin is a cell surface cytotoxic transmembrane protein: ramifications for the complex physiology of TNF". Cell. 53 (1): 45–53. doi:10.1016/0092-8674(88)90486-2. PMID 3349526. S2CID 31789769.
- ^ Tang P, Klostergaard J (1996). "Human pro-tumor necrosis factor is a homotrimer". Biochemistry. 35 (25): 8216–25. doi:10.1021/bi952182t. PMID 8679576.
- ^ Black RA, Rauch CT, Kozlosky CJ, Peschon JJ, Slack JL, Wolfson MF, Castner BJ, Stocking KL, Reddy P, Srinivasan S, Nelson N, Boiani N, Schooley KA, Gerhart M, Davis R, Fitzner JN, Johnson RS, Paxton RJ, March CJ, Cerretti DP (1997). "A metalloproteinase disintegrin that releases tumour-necrosis factor-alpha from cells". Nature. 385 (6618): 729–33. Bibcode:1997Natur.385..729B. doi:10.1038/385729a0. PMID 9034190. S2CID 4251053.
- ^ Palladino MA, Bahjat FR, Theodorakis EA, Moldawer LL (septembar 2003). "Anti-TNF-α therapies: the next generation". Nature Reviews Drug Discovery. 2 (9): 736–46. Bibcode:2003Natur.002..736B. doi:10.1038/nrd1175. PMID 12951580. S2CID 1028523.
- ^ Olszewski MB, Groot AJ, Dastych J, Knol EF (maj 2007). "TNF trafficking to human mast cell granules: mature chain-dependent endocytosis". J. Immunol. 178 (9): 5701–9. doi:10.4049/jimmunol.178.9.5701. PMID 17442953.
In human cells, contrary to results previously obtained in a rodent model, TNF seems not to be glycosylated and, thus, trafficking is carbohydrate independent. In an effort to localize the amino acid motif responsible for granule targeting, we constructed additional fusion proteins and analyzed their trafficking, concluding that granule-targeting sequences are localized in the mature chain of TNF and that the cytoplasmic tail is expendable for endocytotic sorting of this cytokine, thus excluding direct interactions with intracellular adaptor proteins
- ^ Theiss. A. L. et al. 2005. Tumor necrosis factor (TNF) alpha increases collagen accumulation and proliferation in intestinal myofibrobasts via TNF Receptor 2. The Journal of Biological Chemistry. 2005. Available at: http://www.jbc.org/content/280/43/36099.long Accessed: 21/10/14
- ^ Wajant H, Pfizenmaier K, Scheurich P (2003). "Tumor necrosis factor signaling". Cell Death Differ. 10 (1): 45–65. doi:10.1038/sj.cdd.4401189. PMID 12655295.
- ^ Chen G, Goeddel DV (2002). "TNF-R1 signaling: a beautiful pathway". Science. 296 (5573): 1634–5. Bibcode:2002Sci...296.1634C. doi:10.1126/science.1071924. PMID 12040173. S2CID 25321662.
- ^ Kant S, Swat W, Zhang S, Zhang ZY, Neel BG, Flavell RA, Davis RJ (2011). "TNF-stimulated MAP kinase activation mediated by a Rho family GTPase signaling pathway". Genes Dev. 25 (19): 2069–78. doi:10.1101/gad.17224711. PMC 3197205. PMID 21979919.
- ^ Gaur U, Aggarwal BB (2003). "Regulation of proliferation, survival and apoptosis by members of the TNF superfamily". Biochem. Pharmacol. 66 (8): 1403–8. doi:10.1016/S0006-2952(03)00490-8. PMID 14555214.
- ^ Ghada A. Abd El Latif, Tumor necrosis factor alpha and keratin 17 expression in oral submucous fibrosis in rat model, E.D.J. Vol. 65, (1) Pp 277-288; 2019. DOI: 10.21608/edj.2015.71414
- ^ Eastman AJ, Xu J, Bermik J, Potchen N, den Dekker A, Neal LM, et al. (decembar 2019). "Epigenetic stabilization of DC and DC precursor classical activation by TNFα contributes to protective T cell polarization". Science Advances. 5 (12): eaaw9051. doi:10.1126/sciadv.aaw9051. PMC 6892624. PMID 31840058.
- ^ Zhao Z, Lan M, Li J, Dong Q, Li X, Liu B, et al. (april 2019). "The proinflammatory cytokine TNFα induces DNA demethylation-dependent and -independent activation of interleukin-32 expression". The Journal of Biological Chemistry. 294 (17): 6785–6795. doi:10.1074/jbc.RA118.006255. PMC 6497958. PMID 30824537.
- ^ Qi S, Li Y, Dai Z, Xiang M, Wang G, Wang L, Wang Z (decembar 2019). "Uhrf1-Mediated Tnf-α Gene Methylation Controls Proinflammatory Macrophages in Experimental Colitis Resembling Inflammatory Bowel Disease". Journal of Immunology. 203 (11): 3045–3053. doi:10.4049/jimmunol.1900467. PMID 31611260.
- ^ Song M, Fang F, Dai X, Yu L, Fang M, Xu Y (mart 2017). "MKL1 is an epigenetic mediator of TNF-α-induced proinflammatory transcription in macrophages by interacting with ASH2". FEBS Letters. 591 (6): 934–945. doi:10.1002/1873-3468.12601. PMID 28218970.
- ^ Selwood T, Jaffe EK (2011). "Dynamic dissociating homo-oligomers and the control of protein function". Arch. Biochem. Biophys. 519 (2): 131–43. doi:10.1016/j.abb.2011.11.020. PMC 3298769. PMID 22182754.
- ^ Olszewski MB, Groot AJ, Dastych J, Knol EF (maj 2007). "TNF trafficking to human mast cell granules: mature chain-dependent endocytosis". Journal of Immunology. 178 (9): 5701–9. doi:10.4049/jimmunol.178.9.5701. PMID 17442953.
- ^ Gahring LC, Carlson NG, Kulmar RA, Rogers SW (septembar 1996). "Neuronal expression of tumor necrosis factor alpha in the murine brain". Neuroimmunomodulation. 3 (5): 289–303. doi:10.1159/000097283. PMID 9218250.
- ^ Walsh LJ, Trinchieri G, Waldorf HA, Whitaker D, Murphy GF (maj 1991). "Human dermal mast cells contain and release tumor necrosis factor alpha, which induces endothelial leukocyte adhesion molecule 1". Proceedings of the National Academy of Sciences of the United States of America. 88 (10): 4220–4. Bibcode:1991PNAS...88.4220W. doi:10.1073/pnas.88.10.4220. PMC 51630. PMID 1709737.
- ^ Feng P, Jyotaki M, Kim A, Chai J, Simon N, Zhou M, Bachmanov AA, Huang L, Wang H (oktobar 2015). "Regulation of bitter taste responses by tumor necrosis factor". Brain, Behavior, and Immunity. 49: 32–42. doi:10.1016/j.bbi.2015.04.001. PMC 4567432. PMID 25911043.
- ^ Said EA, Dupuy FP, Trautmann L, Zhang Y, Shi Y, El-Far M, Hill BJ, Noto A, Ancuta P, Peretz Y, Fonseca SG, Van Grevenynghe J, Boulassel MR, Bruneau J, Shoukry NH, Routy JP, Douek DC, Haddad EK, Sekaly RP (april 2010). "Programmed death-1-induced interleukin-10 production by monocytes impairs CD4+ T cell activation during HIV infection". Nat. Med. 16 (4): 452–9. doi:10.1038/nm.2106. PMC 4229134. PMID 20208540.
- ^ Starkie R, Ostrowski SR, Jauffred S, Febbraio M, Pedersen BK (2003). "Exercise and IL-6 infusion inhibit endotoxin-induced TNF-α production in humans". FASEB J. 17 (8): 884–886. doi:10.1096/fj.02-0670fje. PMID 12626436. S2CID 30200779.
- ^ Pedersen BK (decembar 2009). "The diseasome of physical inactivity – and the role of myokines in muscle–fat cross talk". J Physiol. 587 (23): 5559–5568. doi:10.1113/jphysiol.2009.179515. PMC 2805368. PMID 19752112.
- ^ Haraoui B, Bykerk V (mart 2007). "Etanercept in the treatment of rheumatoid arthritis". Therapeutics and Clinical Risk Management. 3 (1): 99–105. doi:10.2147/tcrm.2007.3.1.99. PMC 1936291. PMID 18360618.
- ^ Salomon BL, Leclerc M, Tosello J, Ronin E, Piaggio E, Cohen JL (2018). "Tumor Necrosis Factor α and Regulatory T Cells in Oncoimmunology". Front. Immunol. 9: 444. doi:10.3389/fimmu.2018.00444. PMC 5857565. PMID 29593717.
- ^ Korneev KV, Atretkhany KN, Drutskaya MS, Grivennikov SI, Kuprash DV, Nedospasov SA (januar 2017). "TLR-signaling and proinflammatory cytokines as drivers of tumorigenesis". Cytokine. 89: 127–135. doi:10.1016/j.cyto.2016.01.021. PMID 26854213.
- ^ Bouwmeester T, Bauch A, Ruffner H, Angrand PO, Bergamini G, Croughton K, Cruciat C, Eberhard D, Gagneur J, Ghidelli S, Hopf C, Huhse B, Mangano R, Michon AM, Schirle M, Schlegl J, Schwab M, Stein MA, Bauer A, Casari G, Drewes G, Gavin AC, Jackson DB, Joberty G, Neubauer G, Rick J, Kuster B, Superti-Furga G (februar 2004). "A physical and functional map of the human TNF alpha/NF-kappa B signal transduction pathway". Nat. Cell Biol. 6 (2): 97–105. doi:10.1038/ncb1086. PMID 14743216. S2CID 11683986.
- ^ Micheau O, Tschopp J (juli 2003). "Induction of TNF receptor I-mediated apoptosis via two sequential signaling complexes" (PDF). Cell. 114 (2): 181–90. doi:10.1016/S0092-8674(03)00521-X. PMID 12887920. S2CID 17145731.
- ^ Clark IA (June–August 2007). "How TNF was recognized as a key mechanism of disease". Cytokine Growth Factor Rev. 18 (3–4): 335–343. doi:10.1016/j.cytogfr.2007.04.002. hdl:1885/31135. PMID 17493863.
Vanjski linkovi
- "Tasonermin". Drug Information Portal. U.S. National Library of Medicine.
- "Tumor Necrosis Factor-alpha". Drug Information Portal. U.S. National Library of Medicine.
- Tumor Necrosis Factor-alpha na US National Library of Medicine Medical Subject Headings (MeSH)
- P01375
</noinclude>