Triazène
Dans cet article, nous analyserons Triazène sous différentes perspectives afin de comprendre son impact dans différents contextes. Triazène est un sujet qui a suscité un grand intérêt ces dernières années, en raison de sa pertinence dans le domaine social, politique, économique, culturel, entre autres. Tout au long de cette analyse, nous examinerons les différentes dimensions qu'englobe Triazène, ainsi que son évolution dans le temps et son influence sur la société actuelle. De plus, nous explorerons les différentes interprétations et opinions qui existent autour de Triazène, dans le but de fournir une vision large et complète de ce sujet.
| triazène | |
| |
| Identification | |
|---|---|
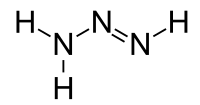
| Nom UICPA | Triazène |
| Synonymes |
Triazanylène |
| No CAS | |
| SMILES | |
| Apparence | gaz odorant |
| Propriétés chimiques | |
| Formule | N3H3 |
| Masse molaire | 45,043 9 ± 0,000 8 g/mol H 6,71 %, N 93,29 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le triazène, aussi connu comme triazanylène, est un composé inorganique insaturé ayant pour formule brute N3H3 ![]() . Il n'est pas présent à l'état naturel.
Le sel déprotoné du triazène comportant une charge négative délocalisée entre les trois N est appelé triazoture (triazide en anglais).
. Il n'est pas présent à l'état naturel.
Le sel déprotoné du triazène comportant une charge négative délocalisée entre les trois N est appelé triazoture (triazide en anglais).
Dérivés

Triazène est aussi le nom générique des dérivés du triazène. Ils contiennent le groupe fonctionnel constitué d'une amine directement liée à un groupe azo, c'est-à-dire R1R2N-N=NR3 où R1, R2 and R3 sont des substituants. Le groupe fonctionnel est aussi appelé groupe diazoamino (mais où seulement un des deux substituants R1 et R3 peut être un hydrogène) parce qu'il est lié au groupe diazo.
Les aryltriazènes, qui sont des espèces stables, peuvent être utilisés comme diazoniums masqués, ces derniers étant très instables. Par simple réaction avec l'acide triflique, un aryltriazène donne un triflate d'aryldiazonium.
Références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- C Picherit, F Wagner, D Uguen, The sequel to a carbocyclic nucleoside synthesis: a divergent access to both arenediazonium ions and aryl triflates, Tetrahedron Letters, 2004, vol. 45(12), pp. 2579-2583. DOI 10.1016/j.tetlet.2004.01.147