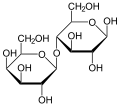
Laktóz
A ma bemutatott cikkünkben a Laktóz lenyűgöző világába fogunk beleásni. A történelem során a Laktóz jelentős hatással volt a társadalom különböző aspektusaira. A populáris kultúrára gyakorolt hatásától a tudományos és technológiai relevanciájáig a Laktóz számtalan területen hagyta nyomát. Ezen a vonalon megvizsgáljuk a Laktóz különböző oldalait, időbeli fejlődését, a modern világra gyakorolt hatását és a jövőre nézve lehetséges következményeit. Csatlakozzon hozzánk ezen az utazáson a Laktóz történetén és társadalmunkra gyakorolt hatásán keresztül.
| Laktóz | |||

| |||
| |||

| |||
| IUPAC-név | β-
d-galaktopiranozil-(1→4)-
d-glükopiranóz | ||
| Más nevek | tejcukor laktobióz α-laktóz β-laktóz β-D-Galp-(1→4)-D-Glcp | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 63-42-3 | ||
| PubChem | 6134 | ||
| ChemSpider | 5904 | ||
| EINECS-szám | 200-559-2 | ||
| KEGG | C01970 | ||
| MeSH | Lactose | ||
| ChEBI | 36218 | ||
| InChIKey | GUBGYTABKSRVRQ-DCSYEGIMSA-N | ||
| Beilstein | 90841 | ||
| Gmelin | 342369 | ||
| UNII | 13Q3A43E0S | ||
| ChEMBL | CHEMBL417016 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C12H22O11 | ||
| Moláris tömeg | 342,296 g/mol | ||
| Megjelenés | színtelen, kristályos anyag[2] fehér por [3] | ||
| Sűrűség | 1,59 g/cm³ (β-laktóz, anhidrát)[3] 1,547 g/cm³ (α-laktóz, monohidrát)[3] 1,525 g/cm³[2] | ||
| Olvadáspont | 252 °C (α-laktóz, anhidrát)[4] 222,8 °C (α-laktóz, anhidrát)[3] 202 °C (α-laktóz, monohidrát)[4] 201 °C (α-laktóz, monohidrát)[3] 252 °C (β-laktóz, anhidrát)[4] 254 °C (β-laktóz, anhidrát)[3] 223 °C[2] | ||
| Oldhatóság (vízben) | Jól oldódik[2] | ||
| Veszélyek | |||
| EU osztályozás | nincsenek veszélyességi szimbólumok[2] | ||
| R mondatok | (nincs)[2] | ||
| S mondatok | (nincs)[2] | ||
| LD50 | > 10000 mg/kg (patkány, szájon át)[2] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A laktóz vagy más néven tejcukor egy diszacharid. A név a tej latin nevéből (lac, lactis) és az '-óz' cukor-végződésből tevődik össze. Az emlősök tejének cukorkomponense a tej szárazanyag-tartalmának kb. 4–7%-át teszi ki.[4] Leginkább tejsavóból vonható ki gazdaságosan.[4] Édes íze van, édesítőereje 68%-a a közönséges cukorénak.[4]
Fizikai és kémiai tulajdonságok
Fehér, szagtalan, enyhén édes ízű, kristályos anyag vagy por.[4] Redukáló hatású vegyület. Vízben nagyon jól, etanolban csekély mértékben oldódik.[3] Dietil-éterben és kloroformban oldhatatlan.[3] Az α- és β-izomer kémiai tulajdonságai megegyezőek, csak fizikai tulajdonságaikban térnek el egymástól, pl. a β-laktóz oldékonyabb, mint az α-laktóz.[5]
Molekulaszerkezet
A molekulában egy galaktóz- és egy glükózmolekula kapcsolódik egymáshoz 1'–4' glikozidos kötéssel. A glükóz lehet α-piranóz vagy β-piranóz formában, míg a galaktóz csak a β-piranóz formában szerepelhet.[5] Ebből kifolyólag az α-laktóz és β-laktóz elnevezés csak a glükopiranóz-gyűrű anomer változataira utal. A gyűrű felnyílása miatt redukáló diszacharid. A belekben található laktáz nevű enzim hidrolizálja, monoszacharidokra bontja. A tej megsavanyodását az okozza, hogy a benne található laktózt baktériumok tejsavvá alakítják. A tej alkoholosan is erjeszthető, ekkor kumisz keletkezik belőle. A laktóz a cellobióztól csak a galaktóz 4-es szénatomjának konfigurációjában tér el.
| A laktóz különböző formái és ábrázolásmódjai | ||
|---|---|---|
| Mills-projekció | Haworth-projekció | |
 α-laktóz |
 α-laktóz | |
 β-laktóz |
 β-laktóz | |
Előfordulás
Megtalálható az emlősök tejében, az Achras sapota gyümölcsében, és még néhány növényben.[4]
Lásd még
Jegyzetek
- ↑ Szénhidrátok nevezéktana http://www.mdche.u-szeged.hu/~kovacs/szhnev/36_k.htm Archiválva 2007. augusztus 16-i dátummal a Wayback Machine-ben
- ↑ a b c d e f g h A laktóz vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. január 12. (JavaScript szükséges) (angolul)
- ↑ a b c d e f g h William M. Haynes. CRC Handbook of Chemistry and Physics, 97th edition, Boca Raton: CRC Press, 3-336. o. (2016). ISBN 978-1-4987-5429-3
- ↑ a b c d e f g h Peter M. Collins. Dictionary of Carbohydrates, 2nd edition, Boca Raton: Chapman & Hall/CRC, 677. o. (2006). ISBN 978-0-8493-3829-8
- ↑ a b Csapó János, Csapóné Kiss Zsuzsanna. Tej és tejtermékek a táplálkozásban. Mezőgazda kiadó (2002). ISBN 978-9-6393-5868-3