Mierenzuur
In de wereld van vandaag is Mierenzuur een onderwerp dat grote relevantie heeft gekregen en de aandacht heeft getrokken van verschillende sectoren van de samenleving. Sinds zijn verschijning heeft Mierenzuur een voor en na gemarkeerd in de manier waarop we met elkaar omgaan, leven en de wereld om ons heen waarnemen. In de loop van de tijd is Mierenzuur een onderwerp van debat en discussie op verschillende gebieden geworden, waardoor tegenstrijdige meningen zijn voortgekomen en acties zijn uitgezet die de levens van mensen hebben beïnvloed. Daarom is het van cruciaal belang om de impact die var1 op ons leven heeft gehad, en op de ontwikkeling van de samenleving als geheel, diepgaand te analyseren en te begrijpen. In dit artikel zullen we enkele facetten van Mierenzuur en de invloed ervan op verschillende aspecten van het dagelijks leven onderzoeken, om zo een breder en uitgebreider beeld te geven van dit uiterst belangrijke onderwerp.
| Mierenzuur | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
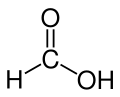
| |||||
Structuurformule van mierenzuur
| |||||

| |||||
Mierenzuur (oplossing van 85% in water)
| |||||
| Algemeen | |||||
| Molecuulformule | of | ||||
| IUPAC-naam | methaanzuur | ||||
| Andere namen | waterstofcarbonzuur, hydrogeencarbonzuur, hydrozine | ||||
| Molmassa | 46,03 g/mol | ||||
| SMILES | C(=O)O
| ||||
| CAS-nummer | 64-18-6 | ||||
| EG-nummer | 200-579-1 | ||||
| Wikidata | Q161233 | ||||
| Beschrijving | Kleurloze vloeistof met een sterke geur | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H226 - H302 - H314 - H331 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P280 - P305+P351+P338 - P310 | ||||
| Hygroscopisch? | ja | ||||
| Omgang | Damp niet inademen, contact vermijden | ||||
| Opslag | Verwijderd houden van ontstekingsbronnen, hitte, vonken en open vlammen Stevig gesloten houden, doch regelmatig druk aflaten: mierenzuur kan druk ontwikkelen. | ||||
| VN-nummer | 1779 | ||||
| MAC-waarde | 9 ml/m3 = 5 ppm | ||||
| LD50 (ratten) | 1100 mg/kg | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vloeibaar | ||||
| Kleur | kleurloos | ||||
| Dichtheid | 1,220 g/cm³ | ||||
| Smeltpunt | 8,4 °C | ||||
| Kookpunt | 100,7 °C | ||||
| Vlampunt | 45 °C | ||||
| Zelfontbrandings- temperatuur | 540 °C | ||||
| Dampdruk | 2800 Pa | ||||
| Goed oplosbaar in | water, ethanol, di-ethylether, glycerol | ||||
| log(Pow) | −0,54 | ||||
| Thermodynamische eigenschappen | |||||
| ΔfH |
−378,6 kJ/mol | ||||
| ΔfH |
−424,72 kJ/mol | ||||
| S |
248,7 J/mol·K | ||||
| S |
128,95 J/mol·K | ||||
| C |
99,04 J/mol·K | ||||
| Evenwichtsconstante(n) | pKa = 3,75 | ||||
| Nutritionele eigenschappen | |||||
| E-nummer | E236 | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Mierenzuur of methaanzuur is een carbonzuur met als brutoformule CH2O2, ook geschreven als HCOOH. Mierenzuur is het eenvoudigste carbonzuur en zeer corrosief. Vroeger was de wetenschappelijke naam dan ook hydrogeencarbonzuur. De zouten en esters van mierenzuur heten formiaten.
Synthese
Mierenzuur kan via enkele stappen uit methanol, water en koolstofmonoxide worden bereid:
- Methanol en koolstofmonoxide reageren bij verhoogde temperatuur en druk tot de ester methylformiaat
- Methylformiaat reageert met water tot mierenzuur en methanol
Daarnaast kan het ook gesynthetiseerd worden, uitgaande van natriumhydroxide, zwavelzuur en koolstofmonoxide:
- Natriumhydroxide en koolstofmonoxide reageren bij verhoogde temperatuur en sterk verhoogde druk tot natriumformiaat
- Natriumformiaat reageert met zwavelzuur tot mierenzuur en natriumsulfaat
DFT-berekeningen suggereren dat rechtstreekse synthese van mierenzuur uit diwaterstof en koolstofdioxide (hydrogenering van CO2) ook mogelijk is dankzij de ontwikkeling van effectieve katalysatoren. Dit is een mogelijke manier om CO2 op te slaan en om te zetten in andere bruikbare verbindingen.
Voorkomen
Mierenzuur komt in veel levende wezens voor, zowel in dieren als in planten. Onder andere mieren maken en gebruiken mierenzuur als middel tot aanval en zelfverdediging, vandaar de naam mierenzuur, maar ook wespen, bijen, hommels en brandnetels verdedigen zich met mierenzuur. In het verleden onttrokken leerlooiers mierenzuur aan mierennesten. Men meende toen dat het de urine van mieren was. Om die reden hebben mieren in sommige dialecten woorden voor urine in hun naam: mieghummel Drents, mierezeiker, zeikmoeier Brabants, aomzeik Limburgs, miegempen Twents.
Zuiver mierenzuur is een gevaarlijke stof omdat het erg corrosief is.
Toepassingen
Industrie
Zuiver mierenzuur is een belangrijke stof in de chemische synthese van veel organische stoffen. Met alcoholen vormt mierenzuur esters (formiaten) die als oplosmiddel of geurstof worden gebruikt. Zuiver mierenzuur dient in schoonmaakmiddelen als antisepticum en ontkalkend middel. Het wordt ook in de leer- en textielindustrie als looi- of beitsmiddel gebruikt.
Waterstofproductie
Mierenzuur is bij proeven toegepast als brandstof voor auto's. Hierbij wordt het mierenzuur (HCOOH) met een katalysator bij kamertemperatuur omgezet in waterstofgas (H2) en kooldioxide (CO2). Met de waterstof kan elektriciteit gegenereerd worden. De omzetting van mierenzuur naar elektriciteit heeft een rendement van ongeveer 45%. De nodige elektriciteit kan op een duurzame manier opgewekt worden, maar deze waterstofproductie is op deze manier nog niet economisch rendabel. Om deze reden wordt waterstof doorgaans geproduceerd op basis van reforming van aardgas.
Het is ook mogelijk mierenzuur rechtstreeks te generen met elektriciteit, water en CO2. Het water wordt in dit proces gebruikt als bron voor de waterstof. Hiermee ontstaat een emissieloze cyclus. Hoewel bij het gebruik van mierenzuur als energiebron CO2 vrijkomt, wordt deze volledig gecompenseerd tijdens de aanmaak van mierenzuur. Het grote voordeel is dat mierenzuur vloeibaar is bij kamertemperatuur en hierdoor gemakkelijker getransporteerd kan worden dan waterstof. Er zijn experimenten gepland met autobussen voorzien van mierenzuurbrandstofcellen.
Hydrozine
Onder de naam Hydrozine produceert sinds 2017 het Team FAST (Formic Acid Sustainable Technologies) van de Technische Universiteit Eindhoven mierenzuur met CO2 uit mest om als brandstof te gebruiken. Als voor de productie duurzame energie wordt gebruikt, heeft men zo een CO2-neutrale brandstof.
Voeding
Mierenzuur en sommige formiaten zijn toegestaan als voedseladditieven. Ze worden gebruikt als conserveermiddel of zuurteregelaar:
- E236 - Mierenzuur
- E237 - Natriumformiaat
- E238 - Calciumformiaat
Externe links
 mierenzuur - International Chemical Safety Card
mierenzuur - International Chemical Safety Card- (en) Gegevens van mierenzuur in de GESTIS-stoffendatabank van het IFA
- (en) MSDS van mierenzuur
Bronnen, noten en/of referenties
|









