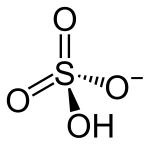
Sulfat
Numera har Sulfat blivit ett brett diskuterat ämne av intresse för både experter och allmänheten. Från dess ursprung till dess påverkan på dagens samhälle har Sulfat varit föremål för många forskningar och debatter inom olika områden. I den här artikeln kommer vi att noggrant utforska vikten av Sulfat, analysera dess olika perspektiv och ge en heltäckande bild av dess relevans i den samtida världen. Från dess inflytande på populärkulturen till dess inverkan på den globala ekonomin, Sulfat förtjänar detaljerad och kritisk uppmärksamhet för att förstå dess verkliga räckvidd i vårt samhälle.
| ||||||||
Sulfater är salter av svavelsyra. Sulfatjonen består av en svavelatom omgiven av fyra syreatomer och är en tetraedrisk tvåvärt negativ jon SO. Sulfat är i allmänhet lättlösliga i vatten undantaget: barium-, strontium-, kalcium-, bly- och kvicksilversulfat. En annan serie sulfat är de sura vätesulfaterna HSO4–; pKa för denna jon är 1,89. Ett exempel på vätesulfat är natriumvätesulfat NaHSO4. När man reducerar sulfatjoner så frigörs svavel och syrgas.
Organiska sulfat
Organiska sulfat, estrarna av svavelsyra, är starkt alkylerande. Det viktigaste är dimetylsulfat (CH3)2SO4, vars användning i Sverige kräver myndighetstillstånd. Salterna av monoförestrade sulfat av typen R-O-SO3– är dock stabila och viktiga surfaktanter.
Sulfatmineral
Flera vanligt förekommande mineral är sulfater. Några är bergartsbildande. Exempel på sulfatmineral är: