Cyclopentanepentone
Dans cet article, nous allons approfondir Cyclopentanepentone, un sujet qui a suscité l'intérêt de nombreuses personnes ces dernières années. Cyclopentanepentone est un sujet d'une grande actualité aujourd'hui et son impact s'est fait sentir dans divers domaines, de la société à la technologie. Depuis longtemps, Cyclopentanepentone fait l’objet de débats et de discussions, tant au niveau académique que dans le grand public. Dans cet article, nous explorerons différents aspects liés à Cyclopentanepentone, en analysant son histoire, son évolution et son influence sur le monde moderne. De plus, nous examinerons les implications de Cyclopentanepentone sur notre vie quotidienne et future.
| Cyclopentanepentone | |
| |
| Identification | |
|---|---|
| Nom UICPA | cyclopentane-1,2,3,4,5-pentone |
| Synonymes |
acide leuconique |
| No CAS | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5O5 [Isomères] |
| Masse molaire | 140,050 5 ± 0,005 5 g/mol C 42,88 %, O 57,12 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
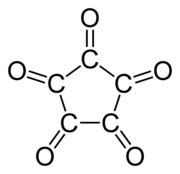
La cyclopentanepentone ou acide leuconique est un composé organique de formule C5O5, soit la quintuple cétone du cyclopentane. C'est un oxyde de carbone, le pentamère du monoxyde de carbone.
En 2000, ce composé n'a pas encore été synthétisé en quantité mais il y a eu des rapports de traces en synthèse,,.
Composés apparentés
La cyclopentanepentone peut être vue comme l'équivalent neutre des anions croconates, C5O52−.
Le composé référencé dans la littérature et le commerce comme la « cyclopentanepentone pentahydrate » (C5O5·5H2O) est probablement le décahydroxycyclopentane (C5(OH)10),.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Cyclopentanepentone » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Mordecai B. Rubin and Rolf Gleite, The Chemistry of Vicinal Polycarbonyl Compounds, Chemical Reviews, 2000, vol. 100(3), pp. 1121–1164. DOI 10.1021/cr960079j.
- (en) Gunther Seitz, « Oxocarbons and pseudooxocarbons », Chemical Reviews, vol. 92, no 6, , p. 1227–1260 (DOI 10.1021/cr00014a004, lire en ligne)
- (en) Detlef Schröder,, « Mass spectrometric studies of the oxocarbons CnOn (n = 3–6) », International Journal of Mass Spectrometry, vol. 188, nos 1–2, , p. 17–25 (DOI 10.1016/S1387-3806(98)14208-2)
- Willis B. Person et Dale G. Williams, "Infrared spectra and the structures of leuconic acid and triquinoyl", J. Phys. Chem., 1957, vol. 61(7), pp. 1017-1018. DOI 10.1021/j150553a047.