Anidride borica
Nell'articolo di oggi approfondiremo l'affascinante mondo di Anidride borica. Che tu stia cercando informazioni su Anidride borica o semplicemente desideri scoprire tutto ciò che questo argomento ha da offrirti, sei nel posto giusto. Dal suo impatto sulla società alle sue varie applicazioni pratiche, esploreremo a fondo ogni aspetto di Anidride borica. Preparati a intraprendere un viaggio di scoperta e apprendimento che ti lascerà con una visione completamente nuova su Anidride borica. Non importa quale sia il tuo livello di conoscenza preliminare su questo argomento, sono sicuro che troverai informazioni nuove e pertinenti che ti saranno molto utili. Iniziamo!
| Anidride borica | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| triossido di diboro | |
| Nomi alternativi | |
| boria | |
| Caratteristiche generali | |
| Formula bruta o molecolare | B2O3 |
| Massa molecolare (u) | 69,6182 g/mol |
| Aspetto | solido bianco cristalli incolori |
| Numero CAS | |
| Numero EINECS | 215-125-8 |
| PubChem | 518682 |
| SMILES | B(=O)OB=O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,460 (20 °C) |
| Costante di dissociazione acida (pKa) a K | ~ 4 |
| Solubilità in acqua | 11 g/l (10 °C) 33 g/l (20 °C) ~ 36 g/l (25 °C) 157 g/l (100 °C) |
| Temperatura di fusione | 450 °C (723 K) |
| Temperatura di ebollizione | 1860 °C (~2133 K) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | -1254 |
| ΔfG0 (kJ·mol−1) | -832 |
| S0m(J·K−1mol−1) | 80.8 |
| C0p,m(J·K−1mol−1) | 66.9 J/mol K |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 3163 mg/kg |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 360 |
| Consigli P | 201 - 202 - 281 - 308+313 - 405 - 501 |
L'anidride borica (nome sistematico: triossido di diboro) è uno degli ossidi del boro, avente formula minima B2O3. Si presenta generalmente come una polvere bianca igroscopica, ma è ottenibile, sebbene non facilmente, anche in forma cristallina incolore. Come materiale ceramico viene detta anche boria. Si trova quasi sempre sotto forma vetrosa (amorfa); tuttavia, può essere cristallizzata dopo un'estesa ricottura (cioè sotto riscaldamento prolungato sotto pressione).
L'anidride borica, insieme alla silice e al carbonato di sodio, è un ingrediente per la produzione di vetri borosilicati.
L'anidride borica è un ossido acido non molto solubile in acqua a freddo, ma comunque reagisce con essa facilmente dando una serie di acidi borici a seconda della concentrazione e della temperatura; in particolare, viene formato il comune acido borico (ortoborico):
B2O3 + 3 H2O → 2 H3BO3
Strutture
Si pensa che lanidride borica vetrosa (γ-B2O3) sia composta da anelli a sei membri, analoghi a quelli della borossina H3B3O3 (o anche della borazina), nei quali c'è un'alternanza di atomi di boro (tricoordinato) e di ossigeno (bicoordinato). A causa della difficoltà di costruire modelli con molti anelli borossinici disordinati ottenendo la densità corretta del materiale, questa visione è stata inizialmente controversa, ma tali modelli sono stati recentemente costruiti e mostrano proprietà in eccellente accordo con i dati sperimentali. È ora riconosciuto, da studi sperimentali e teorici che la frazione di atomi di boro appartenenti agli anelli borossinici nella B2O3 vetrosa è compresa tra 0,73 e 0,83, con 0,75 corrispondente a un rapporto 1:1 tra unità ad anello e unità non ad anello. Il numero di anelli borossinici decade allo stato liquido con l'aumentare della temperatura.
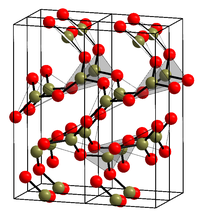
La forma cristallina (si veda la struttura nell'infobox) è composta esclusivamente da triangoli BO3. Questa rete trigonale, simile al quarzo, subisce una trasformazione simile alla coesite in monoclina a diversi gigapascal (9,5 GPa).
Preparazione
L'anidride borica viene prodotta trattando il borace con acido solforico in un forno a fusione. A temperature superiori a 750 °C, lo strato di ossido di boro fuso si separa dal solfato di sodio. Viene quindi decantato, raffreddato e ottenuto con una purezza del 96–97%.
Un altro metodo è il riscaldamento dell'acido borico sopra ~ 300 °C. L'acido borico inizialmente si decompone in vapor d'acqua, (H2O(g)) e acido metaborico (HBO2) a circa 170 °C, e un ulteriore riscaldamento oltre i 300 °C produrrà più vapore e anidride borica. Le reazioni sono:
L'acido borico va al corrispondente microcristallino anidro in un letto fluido riscaldato. La velocità di riscaldamento accuratamente controllata evita la gommatura durante l'evoluzione dell'acqua. L'ossido di boro fuso attacca i silicati. I tubi grafitati internamente tramite decomposizione termica dell'acetilene vengono passivati.
Da un punto di vista cinetico la cristallizzazione dell' fuso a pressione ambiente è fortemente sfavorevole. Le condizioni di soglia per la cristallizzazione del solido amorfo sono 10 kbar e ~200 °C. La sua struttura cristallina proposta nei gruppi spaziali enantiomorfi P31 (gruppo nº144); P32 (gruppo nº145) (ad esempio γ-glicina) è stata rivista nei gruppi spaziali enantiomorfi P3121 (gruppo nº152);P3221 (gruppo nº154)(ad esempio, α-quarzo).
L'anidride borica si formerà anche quando il diborano (B2H6) reagisce con l'ossigeno nell'aria o con tracce di umidità:
Applicazioni
- Agente fondente per vetri e smalti
- Materiale di partenza per la sintesi di altri composti del boro come il carburo di boro
- Additivo utilizzato nelle fibre ottiche
- Componente utilizzato nella produzione di vetro borosilicato
- Lo strato di copertura inerte nel processo Czochralski di incapsulamento liquido per la produzione di monocristallo di arseniuro di gallio
- Come catalizzatore acido nella sintesi organica.
Note
- ^ scheda dell'anidride borica su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ I. Vishnevetsky e M. Epstein, Solar carbothermic reduction of alumina, magnesia and boria under vacuum, in Solar Energy, vol. 111, 1º gennaio 2015, pp. 236–251, DOI:10.1016/j.solener.2014.10.039. URL consultato il 21 aprile 2024.
- ^ I. Vishnevetsky e M. Epstein, Solar carbothermic reduction of alumina, magnesia and boria under vacuum, in Solar Energy, vol. 111, 2015-01, pp. 236–251, DOI:10.1016/j.solener.2014.10.039. URL consultato il 21 aprile 2024.
- ^ Annex XV dossier PROPOSAL FOR IDENTIFICATION OF A SUBSTANCE AS A CATEGORY 1A OR 1B CMR , PBT, vPvB OR A SUBSTANCE OF AN EQUIVALENT LEVEL OF CONCERN, su ECHA, p. 6.
- ^ J. E. Huheey, E. A. Keiter e R. L. Keiter, 16 - Catene, anelli, gabbie e 'clusters' nella chimica inorganica, in Chimica Inorganica, Seconda edizione italiana, sulla quarta edizione inglese, Piccin Nuova Libraria, Padova, 1999, p. 800, ISBN 88-299-1470-3.
- ^ (EN) Ferlat, G., Charpentier, T., Seitsonen, A.P., Takada, A., Lazzeri, M., Cormier, L., Calas, G. e Mauri. F., Boroxol Rings in Liquid and Vitreous B2O3 from First Principles, in Phys. Rev. Lett., vol. 101, n. 6, 2008, p. 065504, DOI:10.1103/PhysRevLett.101.065504.
- ^ (EN) G. Ferlat, A. P. Seitsonen, M. Lazzeri e F. Mauri, Hidden polymorphs drive vitrification in B2O3, in Nature Materials Letters, vol. 11, n. 11, 2012, pp. 925–929, DOI:10.1038/NMAT3416.
- ^ (EN) I. Hung, Determination of the bond-angle distribution in vitreous B2O3 by rotation (DOR) NMR spectroscopy, in Journal of Solid State Chemistry, vol. 182, n. 9, 2009, pp. 2402–2408, DOI:10.1016/j.jssc.2009.06.025.
- ^ (EN) A. K. Soper, Boroxol rings from diffraction data on vitreous boron trioxide, in J. Phys.: Condens. Matter, vol. 23, n. 36, 2011, p. 365402, DOI:10.1088/0953-8984/23/36/365402.
- ^ (EN) C. Joo, The ring structure of boron trioxide glass, in Journal of Non-Crystalline Solids, vol. 261, 1–3, 2000, pp. 282–286, DOI:10.1016/s0022-3093(99)00609-2.
- ^ (EN) J. W. Zwanziger, The NMR response of boroxol rings: a density functional theory study, in Solid State Nuclear Magnetic Resonance, vol. 27, 1–2, 2005, pp. 5–9, DOI:10.1016/j.ssnmr.2004.08.004.
- ^ (EN) M. Micoulaut, The structure of vitreous B2O3 obtained from a thermostatistical model of agglomeration, in Journal of Molecular Liquids, vol. 71, 2–3, 1997, pp. 107–114, DOI:10.1016/s0167-7322(97)00003-2.
- ^ (EN) Alderman, O.L G., Ferlat, G., Baroni, A., Salanne, M., Micoulaut, M., Benmore, C.J., Lin, A., Tamalonis, A. e Weber, J.K.R., Liquid B2O3 up to 1700K: X-ray diffraction and boroxol ring dissolution (PDF), in Journal of Physics: Condensed Matter, vol. 27, n. 45, 2015, p. 455104, DOI:10.1088/0953-8984/27/45/455104.
- ^ (EN) Gurr, G.E., Montgomery, P.W., Knutson, C.D. e Gorres, B.T., The Crystal Structure of Trigonal Diboron Trioxide, in Acta Crystallographica B, vol. 26, n. 7, 1970, pp. 906–915, DOI:10.1107/S0567740870003369.
- ^ (EN) Brazhkin, V.V., Katayama, Y., Inamura, Y., Kondrin, M.V., Lyapin, A.G., Popova, S.V. e Voloshin, R.N., Structural transformations in liquid, crystalline and glassy B2O3 under high pressure, in JETP Letters, vol. 78, n. 6, 2003, pp. 393–397, DOI:10.1134/1.1630134.
- ^ (EN) P. Patnaik, Handbook of Inorganic Chemical Compounds, McGraw-Hill, 2003, p. 119, ISBN 978-00-70-49439-8. URL consultato il 6 giugno 2009.
- ^ (EN) Kocakuşak, S., Akçay, K., Ayok, T., Koöroğlu, H.J., Koral, M., Savaşçi, Ö.T. e Tolun, R., Production of anhydrous, crystalline boron oxide in fluidized bed reactor, in Chemical Engineering and Processing, vol. 35, n. 4, 1996, pp. 311–317, DOI:10.1016/0255-2701(95)04142-7.
- ^ (EN) Morelock, C.R., Research Laboratory Report #61-RL-2672M, General Electric, 1961.
- ^ (EN) Aziz, M.J., Nygren, E., Hays, J.F. e Turnbull, D., Crystal Growth Kinetics of Boron Oxide Under Pressure, in Journal of Applied Physics, vol. 57, n. 6, 1985, p. 2233, DOI:10.1063/1.334368.
- ^ (EN) G.E. Gurr, P.W. Montgomery, C.D. Knutson e B.T. Gorres, The crystal structure of trigonal diboron trioxide, in Acta Crystallographica B, vol. 26, n. 7, 1970, pp. 906–915, DOI:10.1107/S0567740870003369.
- ^ (EN) S.L. Strong, A.F. Wells e R. Kaplow, On the crystal structure of B2O3, in Acta Crystallographica B, vol. 27, n. 8, 1971, pp. 1662–1663, DOI:10.1107/S0567740871004515.
- ^ (EN) H. Effenberger, C.L. Lengauer e E. Parthé, Trigonal B2O3 with Higher Space-Group Symmetry: Results of a Reevaluation, in Monatshefte für Chemie, vol. 132, n. 12, 2001, pp. 1515–1517, DOI:10.1007/s007060170008.
- ^ (EN) AirProducts, Diborane Storage & Delivery (PDF), 2011. URL consultato il 21 agosto 2013 (archiviato dall'url originale il 4 febbraio 2015).
Voci correlate
Altri progetti
 Wikimedia Commons contiene immagini o altri file su anidride borica
Wikimedia Commons contiene immagini o altri file su anidride borica
Collegamenti esterni
- (EN) boric oxide, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | GND (DE) 4146385-7 |
|---|






